题目内容
17.完成下列填空题:(1)写出第二周期元素第一电离能的排列顺序:(用元素符号由低到高排列)LiBBeCONFNe
(2)34Se2-的核外电子排布式:[Ar]3d104s24p6
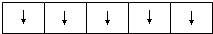
(3)Fe3+的外围电子轨道表示式:
 .
.
分析 (1)同周期随原子序数增大第一电离能呈增大趋势,但第二周期中,铍元素原子2s能级容纳2个电子,处于全满稳定状态,能量较大,失去电子较难,氮元素原子2p能级容纳3个电子,处于半满稳定状态,能量较大,失去电子较难;
(2)原子的左下角为质子数,核外电子数=质子数+得到电子数,根据能量最低原则、泡利不相容原理和洪特规则综合考虑,写出核外电子排布式;
(3)Fe3+的外围电子为3d5,据此书写轨道表示式.
解答 解:(1)同周期随原子序数增大第一电离能呈增大趋势,但第二周期中,铍元素原子2s能级容纳2个电子,处于全满稳定状态,能量较大,失去电子较难,第一电离能高于B元素,氮元素原子2p能级容纳3个电子,处于半满稳定状态,能量较大,失去电子较难,第一电离能高于O元素,故第二周期元素第一电离能的排列顺序由低到高排列的为:Li B Be C O N F Ne,故答案为:Li B Be C O N F Ne;
(2)34Se2-所含质子数为34,原子核外电子数为34+2=36,根据能量最低原则、泡利不相容原理和洪特规则写出为[Ar]3d104s24p6,
故答案为:[Ar]3d104s24p6;
(3)Fe3+的外围电子为3d5,则轨道表示式 ,故答案为:
,故答案为: .
.
点评 本题考查物质结构与性质,涉及核外电子排布、电离能、轨道表示式等,难度中等,注意基础知识的积累.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
7.下列各选项能说明分子式为C4H6的某烃是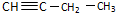 ,而不是
,而不是 的事实是( )
的事实是( )
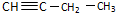 ,而不是
,而不是 的事实是( )
的事实是( )| A. | 燃烧有浓烟 | |
| B. | 能使酸性高锰酸钾溶液褪色 | |
| C. | 所在原子不在同一平面上 | |
| D. | 与足量溴水反应,生成物中只有2个碳原子上有溴原子 |
8.描述CH3-CH=CH-C≡C-CF3分子结构的下列叙述中,正确的是( )
| A. | 6个碳原子有可能都在同一直线上 | |
| B. | 在同一直线上的碳原子可能为4个 | |
| C. | 分子中所有原子有可能都在同一平面上 | |
| D. | 6个碳原子不可能都在同一平面上 |
5.关于10mL 0.1mol•L-1的NH3•H2O溶液,下列说法正确的是( )
| A. | 25℃时,若溶液的pH=11,则Kb(NH3•H2O)=1×10-6 | |
| B. | 向溶液中加入少量CH3COONa固体,溶液中$\frac{c(N{H}_{3}.{H}_{2}O)}{c(N{H}_{4}^{+})}$的值变小 | |
| C. | 向溶液中加入10 mL 0.1 mol•L-1盐酸,所得溶液中离子浓度大小顺序为:c(NH4+)>(Cl-)>c(H+)>c(OH-) | |
| D. | 向溶液中加入5 mL 0.1 mol•L-1盐酸,所得溶液中离子的浓度一定符合:c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
12.某元素原子的N层上只有1或2个电子,则该原子的M层上的电子数可能为( )
| A. | 8 | B. | 18 | C. | 8~18 | D. | 18~32 |
2.化合物X2Y由短周期元素X和Y组成.下列说法一定正确的是( )
| A. | X的原子半径大于Y | |
| B. | 若X为ⅠA族元素,则该化合物中含离子键 | |
| C. | 若X2Y的焰色为黄色,则它的电子式是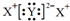 | |
| D. | 若每个X2Y分子中含有10个电子,则Y是第3周期元素 |
9.外围电子构型为4d55s1的元素在周期表中的位置是( )
| A. | 第4周期第ⅠB族 | B. | 第5周期第ⅠB族 | C. | 第4周期第ⅥB族 | D. | 第5周期第ⅥB族 |
6.下列叙述不正确的是( )
| A. | 根据一次能源与二次能源的划分,氢气为二次能源 | |
| B. | 空气、水、煤、天然气均为可再生资源 | |
| C. | 镁条燃烧时将部分化学能转化为光能 | |
| D. | 在火力发电时,化学能转化为热能的过程实际上是氧化还原反应发生的过程,伴随着能量的变化 |
7.反应C(s)+H2O(g)?CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
| A. | 增加C的用量 | B. | 增大反应体系的压强使体积改变 | ||
| C. | 升高体系的反应温度 | D. | 将容器的体积缩小一半 |