题目内容
为探究钢铁的吸氧腐蚀原理设计了如图所示装置,下列有关说法中错误的是 
| A.正极的电极方程式为:O2+2H2O+4e-===4OH- |
| B.将石墨电极改成Mg电极,难以观察到铁锈生成 |
| C.若向自来水中加入少量NaCl(s),可较快地看到铁锈 |
| D.向铁电极附近吹入O2比向石墨电极附近吹入O2,铁锈出现得快 |
D
解析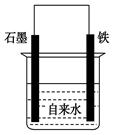
试题分析:A.在钢铁的吸氧腐蚀中,Fe是负极,C作正极,正极的电极方程式为:O2+2H2O+4e-=4OH-,正确;B.若将石墨电极改成Mg电极,由于金属活动性Mg>Fe,Mg作负极,首先被腐蚀,所以难以观察到铁锈生成,正确;C.若向自来水中加入少量NaCl(s),由于溶液中离子的浓度增大,导电性增强,所以可较快地看到铁锈,正确;D.向铁电极附近吹入O2比向石墨电极附近吹入O2,铁锈出现得慢,错误。
考点:考查钢铁的吸氧腐蚀原理的知识。

某学生用0.1000 mol·L-1标准氢氧化钠溶液滴定未知浓度的稀硫酸,其操作可分解为如下几步:
| A.取20.00mL待测硫酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液 |
| B.用标准氢氧化钠溶液润洗滴定管2~3次 |
| C.把盛有标准氢氧化钠溶液碱式滴定管固定好,调节滴定管尖嘴使之充满溶液 |
| D.取标准氢氧化钠溶液注入碱式滴定管至“0”刻度以上2~3mL |
F.把锥形瓶放在滴定管的下面,用标准氢氧化钠溶液滴定至终点并记下滴定管的读数
(1)正确操作步骤的顺序为 (填序号);
(2)上述B步骤操作目的是 ;
(3)判断到达滴定终点的现象是 ;
(4)①达到滴定终点后发现碱式滴定管尖嘴部分有气泡,测定结果会 (填“偏大”“偏小”或“无影响”,下同);
②取待测硫酸溶液的酸式滴定管用蒸馏水洗涤后没有用该硫酸溶液润洗,测定结果会 ;
(5)请在右边的方框内画出正在排气泡的碱式滴定管(仅画出刻度以下部分):

(6)完成3次平行实验,平均消耗标准氢氧化钠溶液体积为20.20mL,则待测液的物质的量浓度为 mol·L-1。
菱镁矿是碱性耐火材料的主要原料,其主要的化学成分是:MgCO3,同时含有杂质:SiO2、Al2O3、Fe2O3、CaO等;目前以菱镁矿为主要原料制备MgSO4的方法如下:
已知:①常温下,Fe3+、Al3+、Mg2+开始形成氢氧化物沉淀和沉淀完全时的pH值如下:
| | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀 | 2.1 | 3.7 | 9.0 |
| 沉淀完全 | 3.2 | 5.2 | 12.4 |
(1)用平衡原理解释:菱镁矿粉粹后加热生成的氧化镁可以溶解在硫酸铵溶液中的原因 。
(2)在该工业流程中,可以循环使用的物质是 。
(3)步骤③中氨气和硫酸恰好完全反应,取此时所得的溶液10.00mL配成250mL溶液,配制溶液过程中除烧杯、玻璃棒、胶头滴管、酸式滴定管外,还需要的玻璃仪器有: ;经检测所配制的溶液pH=1,c(SO42ˉ)=1.05mol/L,试求算所配制溶液中NH4+ 水解的平衡常数K(写计算过程,计算结果保留三位有效数字)。
(4)在加热条件下杂质中的三氧化二铁溶于硫酸铵的离子反应方程式是:
。
(5)蒸发结晶过程中需要使用60~70℃水浴加热方式,其原因是 。
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2=Fe+2Li2S。下列说法不正确的是
| A.可以用水代替SO(CH3)2做溶剂 | B.电子移动方向是由a极流向b极 |
| C.该装置将化学能转化为电能 | D.b极反应式是FeS2+4Li++4e-=Fe+2Li2S |
对铜—锌—稀硫酸组成的原电池装置中,当导线中有1mol电子通过时,理论上的两极变化是①锌片溶解了32.5克 ②锌片增重了32.5克 ③铜片上析出1克氢气④铜片上析出1mol氢气
| A.①③ | B.①④ | C.②③ | D.②④ |
如图,将纯Fe棒和石墨棒插入1 L饱和NaCl溶液中。下列说法正确的是( )
| A.M接负极,N接正极,当两极产生气体总量为22.4 L(标准状况)时,生成1 mol NaOH |
| B.M接负极,N接正极,在溶液中滴人酚酞试液,C电极周围溶液变红 |
| C.M接负极,N接正极,若把烧杯中溶液换成1 L CuSO4溶液,反应一段时间后,烧杯中产生蓝色沉淀 |
| D.M接电源正极,N接电源负极,将C电极换成Cu电极,电解质溶液换成CuSO4溶液,则可实现在铁上镀铜 |
下列防腐措施中,利用原电池反应使主要金属得到保护的是( )
| A.用氧化剂使金属表面生成致密稳定的氧化物保护膜 |
| B.在金属中加入一些铬或镍制成合金 |
| C.在轮船的壳体水线以下部分装上锌锭 |
| D.金属表面喷漆 |
在25ºC时,将两根铂电极插入一定量的硫酸钠饱和溶液中进行电解,当电路中有a mol电子转移时,溶液中析出mg Na2SO4 ·10 H2 O晶体。若温度不变,在剩余溶液中溶质的质量分数为
A.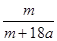 ×100% ×100% | B. ×100% ×100% |
C. ×100% ×100% | D.71m/161(m+9a) ×100% |
据报道,美国正在研究的锌电池可能取代目前广泛使用的铅蓄电池。锌电池具有容量大、污染少等优点。电池反应为2Zn+O2=2ZnO,原料为锌粒、电解液和空气。下列叙述正确的是
| A.锌为正极,空气进入负极反应 |
| B.负极反应为Zn+2OH--2e-=ZnO+H2O |
| C.正极发生氧化反应 |
| D.电解液肯定是强酸 |