题目内容
【题目】金属钛(Ti)被誉为21世纪金属,其单质和化合物具有广泛的应用价值。
(1)在基态Ti原子中,核外存在_____对自旋相反的电子,核外电子占据最高能层的符号是___,占据该能层电子的电子云轮廓图形状为____。
(2)TiCl3 可用作烯烃定向聚合的催化剂,例如丙烯用三乙基铝和三氯化钛做催化剂时,可以发生下列聚合反应:nCH3CH=CH2 ![]()
![]() ,该反应中涉及的物质中碳原子的杂化轨道类型有_______;反应中涉及的元素中电负性最大的是______。 三乙基铝是一种易燃物质,在氧气中三乙基铝完全燃烧所得产物中分子的立体构型是直线形的是__________。
,该反应中涉及的物质中碳原子的杂化轨道类型有_______;反应中涉及的元素中电负性最大的是______。 三乙基铝是一种易燃物质,在氧气中三乙基铝完全燃烧所得产物中分子的立体构型是直线形的是__________。
(3)[TiO(H2O2)2]2+配离子呈黄色。提供中心原子孤电子对的成键原子是_____(填元素符号);配体之一H2O2分子中氧原子的价层电子对互斥模型是___。
(4)科学家通过X射线探明一种氮化钛的晶体与NaCl的晶体结构相似。氮化钛熔点(2950℃)比氯化钠的高,主要原因是________________。
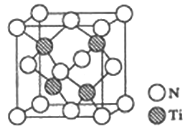
(5)有一种氮化钛晶体的晶胞如图所示,该晶体中Ti原子周围与Ti原子距离最近且相等的N原子的个数为_____。已知晶体的密度为ρ g·cm-3,阿伏加德罗常数为NA,则晶胞边长为____cm(用含ρ、NA的式子表示)。
【答案】10 N 球形 sp2、sp3 Cl CO2 O 四面体形 氮化钛的离子电荷数较多,晶格能较大 4 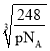
【解析】
(1)Ti位于周期表中第4周期第ⅣB族,核外电子排布式为1s22s22p63s23p63d24s2,则有1+1+3+1+3+1=10对自旋相反的电子;核外有4层,最高电子占据能层为N;占据该能层为s轨道,电子云轮廓图形为球形;
故答案为:10;N;球形;
(2)该反应中存在碳碳双键,碳碳单键,对应的C的杂化方式则有sp2、sp3;反应中涉及的元素有H,C,Al,Cl,Ti,金属元素的电负性较小,非金属元素的电负性较大,且同一周期从左到右,电负性增大,其中电负性最大的是Cl;三乙基铝在氧气中完全燃烧的产物为CO2,Al2O3,H2O,其中直线型的是CO2;
故答案为:sp2、sp3;Cl;CO2;
(3)[TiO(H2O2)2]2+配离子中,O含有孤对电子,能提供孤对电子;对于H2O2,根据VSEPR理论,价电子对数为VP=BP+LP=2+2=4,则O原子为sp3杂化,VSEPR模型为四面体形;
故答案为:O;四面体形;
(4)氮化钛熔点(2950℃)比氯化钠的高,二者结构相似,均为离子晶体,从晶格能角度分析,氮化钛的离子电荷数较多,晶格能较大,熔点更高;
故答案为:氮化钛的离子电荷数较多,晶格能较大;
(5)根据晶胞结构,一个Ti与周围4个N形成四面体结构,所以Ti原子周围与Ti原子距离最近且相等的N原子的个数为4;1个晶胞中含有Ti的个数为4,含有N的个数为8×![]() ++6×
++6×![]() =4个,取1mol这样的晶胞,则1mol晶胞的质量为m=248g,1mol晶胞即含有NA个晶胞,1个晶胞体积为V=a3cm3,则晶体密度为
=4个,取1mol这样的晶胞,则1mol晶胞的质量为m=248g,1mol晶胞即含有NA个晶胞,1个晶胞体积为V=a3cm3,则晶体密度为![]() ,所有晶胞边长为a=
,所有晶胞边长为a=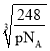 ;
;
故答案为:4;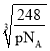 。
。

【题目】在3个体积均为2.0L的恒容密闭容器中,反应CO2(g)+C(s)![]() 2CO(g) H>0分别在一定温度下达到化学平衡状态。下列说法正确的是( )
2CO(g) H>0分别在一定温度下达到化学平衡状态。下列说法正确的是( )
容器 | 温度/K | 起始时物质的量/mol | 平衡时物质的量/mol | ||
n(CO2) | n(C) | n(CO) | n(CO) | ||
Ⅰ | 977 | 0.28 | 0.56 | 0 | 0.4 |
Ⅱ | 977 | 0.56 | 0.56 | 0 | x |
Ⅲ | 1250 | 0 | 0 | 0.56 | y |
A.达到平衡时,向容器Ⅰ中增加C(s)的量,平衡正向移动
B.x=0.8,y>0.4
C.达到平衡时,容器Ⅲ中的CO的转化率小于![]()
D.若起始时向容器Ⅱ中充入0.1molCO2、0.2molCO和足量的C(s),则反应将向正反应方向进行
【题目】已知25℃时,几种常见弱酸的Ka如下表所示:
电解质 | H2C2O4 | CH3COOH | HCN | H2CO3 |
电离常数(molL-1) | K1=5.6×10-2 K2=5.4×10-3 | K=1.7×10-5 | K=6.2×10-10 | K1=4.2×10-7 K2=5.6×10-11 |
(1)草酸(H2C2O4)是一种___(填“一元”、“二元”、“多元”)弱酸。25℃时,0.1molL-1的Na2C2O4、CH3COONa、NaCN、Na2CO3溶液的pH由大到小的顺序是__。
(2)KHC2O4溶液呈酸性,向10mL0.01molL-1的H2C2O4溶液滴加0.01molL-1KOH溶液V(mL)。回答下列问题:
①当V<10mL时,反应的离子方程式为___。
②当V=10mL时,溶液中![]() 、
、![]() 、H2C2O4、H+的浓度由大到小的顺序为__。
、H2C2O4、H+的浓度由大到小的顺序为__。
③当V=amL时,溶液中离子浓度有如下关系:c(K+)=2c(![]() )+c(
)+c(![]() );当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(
);当V=bmL时,溶液中离子浓度有如下关系:c(K+)=c(![]() )+c(
)+c(![]() )+c(H2C2O4);则a__b(填“<”“=”或“>”).
)+c(H2C2O4);则a__b(填“<”“=”或“>”).
【题目】根据下列实验操作和现象所得到的结论正确的是( )
选项 | 实验操作和现象 | 结论 |
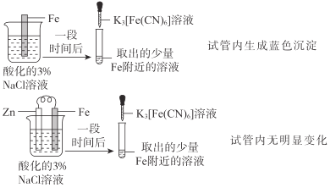
A |
| Zn保护了Fe不被腐蚀 |
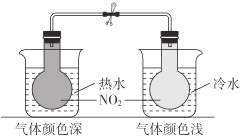
B |
| 2NO2(g)N2O4(g)为吸热反应 |
C |
| 木炭与浓硝酸发生了反应 |
D |
| 碳酸钠的水解程度强 |
A.AB.BC.CD.D