题目内容
6.能正确表示下列反应的离子(或化学)方程式是 ( )| A. | 金属Al溶于稀硝酸中:2Al+6H+═2Al3++3H2↑ | |
| B. | CuH在足量C12中燃烧:2CuH+2Cl2$\frac{\underline{\;点燃\;}}{\;}$2CuCl2+H2 | |
| C. | 向复盐NH4Al(S04)2溶液中加入Ba(0H)2至沉淀质量最大:NH4++Al3++4OH-+2SO42-═NH3•H2O+Al(OH)3↓+2BaSO4↓ | |
| D. | 向饱和NaHSO3溶液中加入FeC13溶液:S032-+2Fe3++H20═S042-+2Fe2++2H+ |
分析 A.铝与稀硝酸反应生成NO气体,不会生成氢气;
B.氯气足量,点燃条件下氢气会与氯气反应生成氯化氢;
C.铵根离子结合氢氧根离子能力大于氢氧化铝,所以沉淀足量最大时,反应生成氢氧化铝、硫酸钡沉淀和一水合氨;
D.亚硫酸氢根离子不能拆开.
解答 解:A.金属铝溶于稀硝酸中生成NO气体,正确的离子反应为:NO3-+Al+4H+=A13++NO↑+2H2O,故A错误;
B.CuH在足量C12中燃烧生成氯化铜和氯化氢,正确的化学方式为:2CuH+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2CuCl2+2HCl,故B错误;
C.两溶液混合后NH4+、Al3+与OH-都能反应,OH-先与Al3+反应,当溶液中Al3+完全转化成氢氧化铝沉淀后,才发生NH4+与OH-的反应,沉淀质量最大时的离子方程式为:NH4++Al3++4OH-+2SO42-═NH3•H2O+Al(OH)3↓+2BaSO4↓,故C正确;
D.饱和NaHSO3溶液中加入FeC13溶液,亚硫酸氢根离子不能拆开,正确的离子方程式为:HS03-+2Fe3++H20═S042-+2Fe2++3H+,故D错误;
故选C.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,注意明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
17.在体积相同的三个密闭容器中分别充入Ne、H2、O2三种气体,当它们的温度与密度都相同时,这三种气体的分子数(N)由多到少的顺序是( )
| A. | N(Ne)>N(H2)>N(O2) | B. | N(O2)>N(Ne)>N(H2) | C. | N(H2)>N(O2)>N(Ne) | D. | N(H2)>N(Ne)>N(O2) |
11.在氯水中存在多种分子和离子,它们在不同的反应中表观各自的性质,下列实验观象和结论一致且正确的是( )
| A. | 加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在 | |
| B. | 新制氯水可使蓝色石蕊试纸先变红后褪色 | |
| C. | 氯气长时间放置后酸性减弱 | |
| D. | 加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在 |
15.下列说法中正确的是( )
| A. | CuSO4 •5H2O 是混合物 | |
| B. | 含Fe元素质量分数为70%的Fe2O3是纯净物 | |
| C. | 冰和水混合在一起形成混合物 | |
| D. | 由单质形成的物质一定是纯净物 |
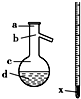 实验室中用苯甲醛制备苯甲醇和苯甲酸,已知反应原理:2HCHO+KOH-→CH3OH+HCOOK
实验室中用苯甲醛制备苯甲醇和苯甲酸,已知反应原理:2HCHO+KOH-→CH3OH+HCOOK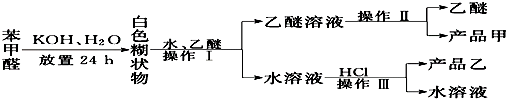
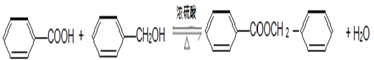 ,实验室在收集此特殊香味的物质时常用饱和Na2CO3溶液 (填试剂名称)除去其中的杂质,且便于其分层析出.
,实验室在收集此特殊香味的物质时常用饱和Na2CO3溶液 (填试剂名称)除去其中的杂质,且便于其分层析出.