题目内容
14.用一种试剂除去下列各物质中的杂质(括号内为杂质),写出所用试剂以及发生反应的离子方程式.(1)BaCl2(HCl)试剂BaCO3粉末;化学方程式为BaCO3+2H+═Ba2++CO2↑+H2O
(2)Cu(Fe)试剂盐酸;化学方程式为Fe+2H+=Fe2++H2↑
(3)Na2SO4 (Na2CO3)稀硫酸;化学方程式为CO32-+2H+═H2O+CO2↑.
分析 (1)可用BaCO3粉末与盐酸反应除杂;
(2)铁为活泼技术,可与盐酸反应而除去;
(3)可加入硫酸,反应生成二氧化碳气体.
解答 解:(1)BaCO3粉末能与盐酸反应生成氯化钡、水和二氧化碳,且BaCO3粉末不溶于水,过滤除去,能除去杂质且没有引入新的杂质,符合除杂原则,反应的离子方程式为BaCO3+2H+═Ba2++CO2↑+H2O,
故答案为:BaCO3粉末;BaCO3+2H+═Ba2++CO2↑+H2O;
(2)铁为活泼金属,可与盐酸反应而除去,反应的离子方程式为Fe+2H+=Fe2++H2↑,故答案为:盐酸;Fe+2H+=Fe2++H2↑;
(3)硫酸的酸性比碳酸强,可选用稀硫酸除去Na2CO3,离子方程式为:CO32-+2H+═H2O+CO2↑,故答案为:稀硫酸;CO32-+2H+═H2O+CO2↑;
点评 本题考查离子反应及物质的除杂,为高频考点,把握物质的性质及发生的离子反应为解答的关键,注意除杂时选择试剂不能引入新杂质,题目难度不大.

练习册系列答案
相关题目
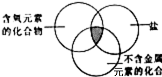
5.下列物质符合如图阴影部分的要求,且其在水溶液中的电离方程式书写正确的是( )

| A. | K2CO3═2K++CO32- | B. | NH4NO3═NH4++NO3- | ||
| C. | H2SO4═2H++SO42- | D. | NH4ClO3═NH4++Cl5++3O2- |
2.下列离子组中,在由水电离出的c(H+)•c(0H-)=1×10-26mol•L-1的溶液中一定能大量共存的是( )
| A. | Na+、Mg2+、Al3+、Cl- | B. | Na+、K+、Cl-、SO42- | ||
| C. | HCO3-、Na+、Cl-、K+ | D. | I-、Fe2+、Na+、NO3- |
9.物质的量浓度相同的下列物质的水溶液,H+浓度最小的是( )
| A. | Na2C03 | B. | HCl | C. | Na2S04 | D. | KN03 |
19.已知某二元酸H2A溶于水发生电离:H2A=H++HA-;HA-?H++A2-,则酸式盐MHA溶于水电离出的离子中,一定不能发生水解的是( )
| A. | M+ | B. | HA- | C. | A2- | D. | M+和HA- |
6.能正确表示下列反应的离子(或化学)方程式是 ( )
| A. | 金属Al溶于稀硝酸中:2Al+6H+═2Al3++3H2↑ | |
| B. | CuH在足量C12中燃烧:2CuH+2Cl2$\frac{\underline{\;点燃\;}}{\;}$2CuCl2+H2 | |
| C. | 向复盐NH4Al(S04)2溶液中加入Ba(0H)2至沉淀质量最大:NH4++Al3++4OH-+2SO42-═NH3•H2O+Al(OH)3↓+2BaSO4↓ | |
| D. | 向饱和NaHSO3溶液中加入FeC13溶液:S032-+2Fe3++H20═S042-+2Fe2++2H+ |
8. 某实验小组利用如下装置合成正丁醛.发生的反应如下:
某实验小组利用如下装置合成正丁醛.发生的反应如下:
CH3CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90~95℃,在E中收集90℃以上的馏分.
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g.回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,浓硫酸溶于水会放出大量热,容易溅出伤人.
(2)加入沸石的作用是防止暴沸.
(3)上述装置图中,B仪器的名称是分液漏斗,D仪器的名称是直形冷凝管.
(4)反应温度应保持在90~95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
(5)温度计C1的作用测量烧瓶中反应物的温度,C2的作用测量馏分的沸点.
 某实验小组利用如下装置合成正丁醛.发生的反应如下:
某实验小组利用如下装置合成正丁醛.发生的反应如下:CH3CH2CH2OH$→_{H_{2}SO_{4}△}^{Na_{2}Cr_{2}O_{7}}$CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
| 沸点/℃ | 密度/g•cm-3 | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中.在A中加入4.0g正丁醇和几粒沸石,加热.当有蒸汽出现时,开始滴加B中溶液.滴加过程中保持反应温度为90~95℃,在E中收集90℃以上的馏分.
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77℃馏分,产量2.0g.回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由不能,浓硫酸溶于水会放出大量热,容易溅出伤人.
(2)加入沸石的作用是防止暴沸.
(3)上述装置图中,B仪器的名称是分液漏斗,D仪器的名称是直形冷凝管.
(4)反应温度应保持在90~95℃,其原因是保证正丁醛及时蒸出,又可尽量避免其被进一步氧化.
(5)温度计C1的作用测量烧瓶中反应物的温度,C2的作用测量馏分的沸点.
 .
.