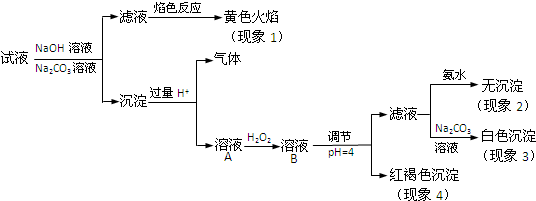
题目内容
4.设NA为阿伏加德岁常数的值,下列叙述正确的是( )| A. | 标准状况下,33.6L氟化氢中含有氟原子的数目为1.5NA | |
| B. | 常温常压下,7.0g乙烯与丙烯的混合物中含有碳氢键的数目为NA | |
| C. | 50 mL18.4mol/L浓硫酸与足量铜微热反应,生成S02分子的数目为0.46NA | |
| D. | 某密闭容器盛有0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目为0 6NA |
分析 A、标况下,HF为液体;
B、乙烯和丙烯均由CH2构成;
C、铜只能与浓硫酸反应,与稀硫酸不反应;
D、合成氨的反应为可逆反应.
解答 解:A、标况下,HF为液体,故不能根据气体摩尔体积来计算其物质的量,故A错误;
B、乙烯和丙烯均由CH2构成,故7.0g混合物中含有的CH2的物质的量n=$\frac{7g}{14g/mol}$=0.5mol,故含有1molC-H键即NA个,故B正确;
C、铜只能与浓硫酸反应,与稀硫酸不反应,故硫酸不能反应完全,则生成的二氧化硫分子个数小于0.46NA个,故C错误;
D、合成氨的反应为可逆反应,故不能反应完全,则转移的电子数小于0.6NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
1.下列各溶液中能大量共存的离子组是( )
| A. | 在碱性溶液中:Na+,NO3-,S2-,SO32- | |
| B. | 使pH试纸呈红色的溶液中:Fe2+,I-,NO3-,Cl- | |
| C. | 碳酸氢钠溶液中:K+,SO42-,Cl-,H+ | |
| D. | 使酚酞试液呈红色的溶液中:Mg2+,Cu2+,SO42-,K+ |
12.向四支试管中分别加入少量不同的无色溶液进行如下操作,则有关操作、现象、结论的描述均正确的是( )
| 操作 | 现象 | 结论 | |
| A | 先滴加BaCl2溶液再滴加HCl溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B | 加CCl4,振荡、静置 | 上层溶液显紫色 | 原溶液中有I2 |
| C | 滴加NaOH溶液,将湿润 红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
| D | 用洁净铁丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+ |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
19.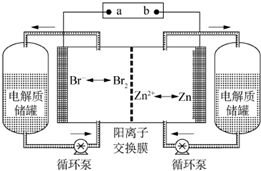 锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环.下列说法不正确的是( )
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环.下列说法不正确的是( )
 锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环.下列说法不正确的是( )
锌溴液流电池是一种新型电化学储能装置(如图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环.下列说法不正确的是( )| A. | 充电时,阳离子通过交换膜移向装置右侧 | |
| B. | 充电时,左侧与右侧的溴化锌溶液的浓度差将减小 | |
| C. | 放电时装置发生的总反应为:Zn+Br2═ZnBr2 | |
| D. | 阳离子交换膜可阻止Br2与Zn直接发生反应 |
16.不能用单质直接化合而得到的化合物是( )
| A. | FeCl2 | B. | Al2S3 | C. | CuCl2 | D. | Mg3N2 |
13.医学上通过放射性14C标记的C60进行跟踪研究,发现一种C60的羧酸衍生物在特定的条件下可通过断裂DNA杀死细胞,从而抑制艾滋病.有关C60和14C的叙述正确的是( )
| A. | 12C与14C互为同素异形体 | |
| B. | 14C的原子中有6个质子,8个电子 | |
| C. | 12C与14C的原子中含有的中子数之比为3:4 | |
| D. | 金刚石与C60都属于原子晶体 |
14.下列叙述中,你认为科学的是( )
| A. | 在地球上分布很广,淡水资源取之不尽,用之不竭 | |
| B. | 大气中二氧化碳含量的增多是造成“温室效应”的主要原因 | |
| C. | 某广告语:本饮料纯属天然物质,不含任何化学成分 | |
| D. | 到城乡结合处燃放鞭炮,可避免污染环境 |