题目内容
【题目】下列有关溶液中粒子浓度的关系式中,正确的是( )

A.pH相同的①CH3COONa、②NaHCO3、③Na2CO3三份溶液中的c(Na+):③>②>①
B.0.1mol·L-1某二元弱酸强碱盐NaHA溶液中:c(Na+)=2c(A2-)+c(HA-)+c(H2A)
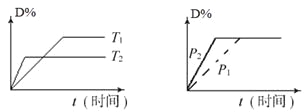
C.图中a点溶液中各离子浓度的关系是:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)
D.图中pH=7时:c(Na+)>c(CH3COO-) >c(OH-)=c(H+)
【答案】C
【解析】
A.pH相同的钠盐溶液中,弱根离子水解程度越大,其盐溶液浓度越小,碳酸钠的水解程度大于碳酸氢钠,大于醋酸钠,则当三种溶液的pH相同时,其物质的量浓度由大到小的顺序是③<②<①,钠离子浓度大小顺序是③<②<①,故A错误;
B.根据物料守恒得c(Na+)=c(A2-)+c(HA-)+c(H2A),故B错误;
C.a点溶液中存在的溶质是等物质的量的醋酸钠和氢氧化钠,根据物料守恒得c(Na+)=2c(CH3COO-)+2c(CH3COOH),根据电荷守恒得c(Na+)+c(H+)=c(CH3COO-)+c(OH-),所以得c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH),故C正确;
D.pH=7时c(OH-)=c(H+),溶液中存在电荷守恒c(Na+)+c(H+)=c(CH3COO-)+c(OH-),所以得c(Na+)=c(CH3COO-),故D错误;
故选:C。

 名师指导期末冲刺卷系列答案
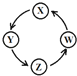
名师指导期末冲刺卷系列答案【题目】下列各组物质中,满足表中图示物质在一定条件下能一步转化的组合有
序号 | X | Y | Z | W |
|
① | Cu | CuSO4 | Cu(OH)2 | CuO | |
② | Na | NaOH | Na2CO3 | NaCl | |
③ | Al | AlCl3 | Al(OH)3 | Al2O3 | |
④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
A. ②③ B. ①③④ C. ①④ D. ①②③