题目内容
10.下列各原子或离子的电子排布式错误的是( )| A. | Ca2+ 1s22s22p63s23p6 | B. | O2-1s22s23p4 | ||
| C. | Cl- 1s22s22p63s23p6 | D. | Ar 1s22s22p63s23p6 |
分析 主族元素原子失去电子变成阳离子时,核外电子数、电子层数、最外层电子数改变;主族元素原子得到电子变成阴离子时,核外电子数和最外层电子数改变,但电子层数不变.
解答 解:A、钙原子失去2个电子变成钙离子,使次外层变成最外层,所以钙离子核外有18个电子,故A正确;
B、氧原子核外有8个电子,氧原子得2个电子变成氧离子,最外层电子数由6个变成8个,所以氧离子核外有10电子,故B错误;
C、氯原子核外有17个电子,氯原子得一个电子变成氯离子,最外层由7个电子变成8个电子,所以氯离子核外有18个电子,故C正确;
D、氩是18号元素,原子核外有18个电子,故D正确.
故选B.
点评 本题考查了原子或离子的核外电子排布,难度不大,明确原子变成阴、阳离子时变化的量是解本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.下列为元素周期表中的一部分,用化学式或元素符号回答下列问题:
(1)①②⑤中,最高价氧化物对应水化物,碱性最强的是KOH.
(2)②③⑧中形成的简单离子半径由大到小的顺序是Cl->K+>Mg2+.
(3)①和⑨两元素形成的化合物的溶液与元素⑧的单质反应的离子方程式为Cl2+2Br-=Br2+2Cl-.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | ⑥ | ⑦ | ||||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(2)②③⑧中形成的简单离子半径由大到小的顺序是Cl->K+>Mg2+.
(3)①和⑨两元素形成的化合物的溶液与元素⑧的单质反应的离子方程式为Cl2+2Br-=Br2+2Cl-.
5.工业上常用氯气给自来水消毒.某学生用自来水配制下列物质的溶液,不会产生明显药品变质的是( )
| A. | 氯化铝 | B. | 石蕊 | C. | 亚硫酸钠 | D. | 硝酸银 |
15.下列说法正确的是( )
| A. | pH=2与pH=1的硝酸中c(H+)之比为1:10 | |
| B. | Na2CO3溶液中c(Na+)与c(CO32-)之比为2:1 | |
| C. | 0.2 mol•L-1与0.1mol/L醋酸中c (H+)之比为2:1 | |
| D. | NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为3:1 |
2.普伐他汀是一种调节血脂的药物,其结构简式如图所示.下列关于普伐他汀的性质描述正确的是( )
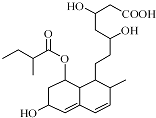

| A. | 能与FeCl3 溶液发生显色反应 | |
| B. | 能使酸性KMnO4 溶液褪色 | |
| C. | 不能发生加成、取代、消去反应 | |
| D. | 1mol 该物质最多可与3mol NaOH 反应 |
19.在稀硫酸酸化的H2O2溶液中加入乙醚(C2H5-O-C2H5)后,溶液分层,再加入少量K2Cr2O7溶液,并振荡,在乙醚层中出现深蓝色,这是因为生成2CrO5•(C2H5)2O所致,其反应方程式为:Cr2O72-+4H2O2+2H+═2CrO5+5H2O,已知:CrO5的结构式为: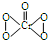 下列说法正确的是( )
下列说法正确的是( )
 下列说法正确的是( )
下列说法正确的是( )| A. | Cr2O72- 被氧化成CrO5 | |
| B. | 该反应为氧化还原反应 | |
| C. | 反应中H2O2被还原成H2O | |
| D. | 此反应用于检验Cr2O72-离子的存在 |