题目内容
9.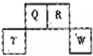 短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列说法正确的是( )
短周期元素Q、R、T、W在元素周期表中的位置如图所示,其中T所处的周期序数与主族序数相等,下列说法正确的是( )| A. | W在周期表中的位置是第三周期,ⅤA族 | |
| B. | 原子半径Q>R>T | |
| C. | W原子得电子能力强于Q原子,且可形成共价化合物QW2 | |
| D. | 原子序数比R多1的元素只有一种氢化物 |
分析 由短周期元素Q、R、T、W在元素周期表中的位置,可知Q、R处于第二周期,T、W处于第三周期,T所处的周期序数与主族序数相等,则T为Al,可推知Q为C元素、R为N元素、W为S元素.
A.主族元素周期数=电子层数、族序数=最外层电子数;
B.同周期自左而右原子半径减小、同主族自上而下原子半径增大;
C.碳酸属于弱酸,硫酸属于强酸,则S元素电子能力比碳的强,碳元素与硫元素可形成共价化合物CS2;
D.原子序数比R多1的元素为氧,其氢化物有水、过氧化氢.
解答 解:由短周期元素Q、R、T、W在元素周期表中的位置,可知Q、R处于第二周期,T、W处于第三周期,T所处的周期序数与主族序数相等,则T为Al,可推知Q为C元素、R为N元素、W为S元素.
A.W为硫元素,原子核外有3个电子层,最外层电子数为6,处于第三周期VIA族,故A错误;
B.同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径T>Q>R,故B错误;
C.碳酸属于弱酸,硫酸属于强酸,则S元素电子能力比碳的强,碳元素与硫元素可形成共价化合物CS2,故C正确;
D.原子序数比R多1的元素为氧,其氢化物有H2O、H2O2,故D错误,
故选:C.
点评 本题考查结构性质位置关系应用,难度不大,注意掌握金属性、非金属性强弱比较及微粒半径比较.

练习册系列答案
相关题目
20.溴、碘主要存在于海水中,有“海洋元素”的美称,海水中的碘富集在海藻中,我国海带产量局世界第一,除供食用外,大量用于制碘,提取碘的途径如下所示:
干海带$\stackrel{焙烧}{→}$海带灰$\stackrel{水}{→}$水溶液$\stackrel{氧化}{→}$$\stackrel{A}{→}$$\stackrel{B}{→}$→碘单质
下列有关叙述不正确的是( )
干海带$\stackrel{焙烧}{→}$海带灰$\stackrel{水}{→}$水溶液$\stackrel{氧化}{→}$$\stackrel{A}{→}$$\stackrel{B}{→}$→碘单质
下列有关叙述不正确的是( )
| A. | 碘元素在海水中没有游离态存在 | |
| B. | 在提取的过程中用的氧化剂可以是H2O2 | |
| C. | 操作A是萃取 | |
| D. | B是提纯操作,常用蒸馏 |
19.设阿伏加德罗常数的数值为NA,下列说法正确的是( )
| A. | 2.3 g Na和足量的O2完全反应,生成3.4g固体混合物,转移电子数为0.1NA | |
| B. | 电解精炼铜时,当阳极减少64g金属时转移的电子数为2NA | |
| C. | 46 g的NO2与46 g的N2O4含有的原子数不同 | |
| D. | 标准状况下,11.2 L苯中含有碳碳双键数目为3NA |
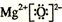 .
.


