题目内容
【题目】CO2的资源化利用能有效减少CO2的排放,充分利用碳资源。
(1)全球变暖现象很可能是大气中的温室气体(如CO2)聚集造成的。有科学家提出可以将CO2通过管道输送到海底,这样可减缓空气中CO2浓度的增加。下列有关说法正确的是__(填字母)。
A.送到海底越深的地方,CO2溶解得越多,同时CO2可能液化甚至变成干冰
B.把CO2输送到海底,会使海水酸性增强,有利于海洋生态环境
C.把CO2输送到海底,这是人类减缓空气中CO2浓度增加速率的唯一办法
D.要减缓空气中CO2浓度的增加,最有效的措施是使用新能源和植树造林
(2)已知:①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890kJ·mol-1
②2H2(g)+O2(g)=2H2O(l) ΔH=-572kJ·mol-1
则反应CO2(g)+4H2(g)=CH4(g)+2H2O(l) ΔH=__kJ·mol-1。
(3)CO2催化加氢合成二甲醚是CO2转化的一种方法,主要发生下列反应:
反应Ⅰ:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41.2kJ·mol-1
反应Ⅱ:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ΔH=-122.5kJ·mol-1
在一体积为1L的恒容密闭容器中,充入1molCO2与1molH2,CO2的平衡转化率和平衡时CH3OCH3的选择性随温度的变化曲线如图所示。其中:CH3OCH3的选择性=![]() ×100%。
×100%。
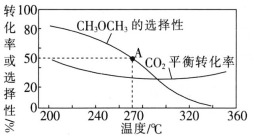
①CH3OCH3的选择性随温度的升高而降低的原因是___。
②270℃时,测得平衡时CH3OCH3的物质的量为0.1mol,此时反应Ⅰ的化学平衡常数K=__(保留2位有效数字)。
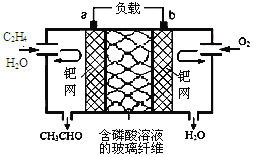
(4)多晶Cu是目前唯一被实验证实能高效催化CO2还原为烃类(如C2H4)的金属。电解装置中分别以多晶Cu和铂为电极材料,用阴离子交换膜分隔开阴、阳极室,阴、阳极室的KHCO3溶液的浓度(约0.1mol·L-1左右)基本保持不变。并向某极室内持续通入CO2,温度控制在10℃左右。通入CO2的电极为___(填“阴极”或“阳极”),生成C2H4的电极反应式为__。
【答案】AD -254 反应I的△H>O,反应Ⅱ的△H<0,温度升高,反应I正向进行,反应Ⅱ逆向进行,CH3OCH3的选择性降低 0.83 阴 14CO2+12e-+8H2O=C2H4+12HCO3-
【解析】
(1)从影响环境的角度考虑;
(2)根据盖斯定律进行分析;
(3)利用化学平衡常数的表达式进行分析;
(4)利用电解原理、电极反应式的书写;
(1)A、气体溶解度随压强的增大而增大,压强增大CO2可能液化,故A说法正确;
B、CO2能与水反应生成H2CO3,使海水酸性增强,破坏海洋生态环境,故B说法错误;
C、减缓空气中CO2浓度有多种方法,如合成聚二氧化碳塑料等,故C说法错误;
D、使用新能源减少CO2排放,植树造林可降低CO2浓度,故D说法正确;
答案为AD;
(2)利用盖斯定律,根据目标反应方程式,有②×2-①,△H=(-572×2kJ·mol-1)-(-890kJ·mol-1)=-254kJ·mol-1;
答案为-254kJ·mol-1;
(3)①反应I△H>0,属于放热反应,升高温度,平衡正向移动,反应Ⅱ的△H<0,该反应为放热反应,升高温度,平衡逆向进行,CH3OCH3的选择性降低;
答案为反应I的△H>O,反应Ⅱ的△H<0,温度升高,反应I正向进行,反应Ⅱ逆向进行,CH3OCH3的选择性降低;
②根据图像,在270℃时,CH3OCH3的选择性为50%,测的平衡时CH3OCH3的物质的量为0.1mol,依据CH3OCH3的选择性公式计算出反应中消耗CO2的物质的量为0.4mol,则剩余CO2的物质的量为(1-0.4)mol=0.6mol,因此有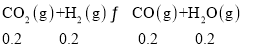
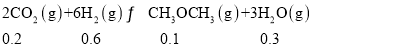 达到平衡后n(H2O)=0.5mol,n(H2)=(1-0.8)mol=0.2mol,n(CO)=0.2mol,根据化学平衡常数的表达式,K=
达到平衡后n(H2O)=0.5mol,n(H2)=(1-0.8)mol=0.2mol,n(CO)=0.2mol,根据化学平衡常数的表达式,K=![]() ,代数数值K≈0.83;
,代数数值K≈0.83;
答案为0.83;
(4)根据题意CO2→C2H4,C的化合价由+4价→-2价,化合价降低,根据电解原理,通入CO2的电极为阴极,其电极反应式为14CO2+12e-+8H2O=C2H4+12HCO3-;
答案为阴极;14CO2+12e-+8H2O=C2H4+12HCO3-。

【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | M层上电子数是K层上电子数的3倍 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
(1)元素X在元素周期表中的位置为:___,它的一种核素可测定文物年代,这种核素的符号是___。
(2)元素Y的原子结构示意图为___,Y与氢元素形成一种离子YH4+,写出某溶液中含有该微粒的检验方法__。
(3)元素Z与元素T相比,非金属性较强的是__(用元素符号表示),下列表述中能证明这一事实的是___(填字母)。
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应
(4)X的最高价氧化物的结构式为__。