题目内容
【题目】298K时,1mol N2与3mol H2完全反应生成2molNH3的能量变化曲线如图,下列叙述正确的是
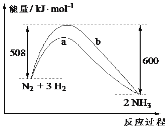
A.形成6 mol N—H键,吸收600 kJ能量
B.b曲线是加入催化剂时的能量变化曲线
C.该反应的ΔH=-92 kJmol-1
D.加入催化剂,能提高N2的转化率
【答案】C
【解析】
A.由图可知,反应为放热反应,故 形成6 mol N-H键,放出600 kJ能量,A错误;
B. 催化剂能降低反应的活化能,b曲线是未加入催化剂时的能量变化曲线,B错误;
C. 该反应的ΔH=(508-600) kJmol-1=-92 kJmol-1,C正确;
D. 使用催化剂只能缩短到达平衡的时间,不能提高N2的转化率,D错误。
故选C。

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目