题目内容
【题目】兴趣小组分析了用硫铁矿烧渣(主要成份Fe2O3、Fe3O4、FeO等)制备铁红(Fe2O3)的流程图并进行了铁红性质实验。
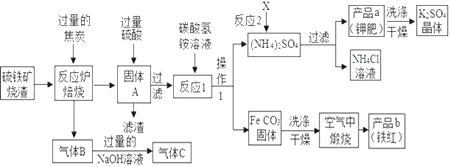
(1)写出焙烧中一氧化碳与氧化铁反应的化学方程式___________。
(2)实验室完成操作1,用到的玻璃仪器有烧杯、玻璃棒和_______(填仪器名称)。
(3)你认为对气体C最佳的处理方法是________。
A.冷却后排入空气B.燃烧后排放C.再通入反应炉
(4)反应1的反应温度一般需控制在35℃以下,其目的是___________。
(5)反应2中相关物质的溶解度如表,你认为该反应在常温下能实现的原因是:________。

洗涤干燥得到硫酸钾晶体时,可选用下列______(选填序号,下同)洗涤剂
A.氯化钾饱和溶液 B.水 C.硫酸钾饱和溶液
为检验硫酸钾晶体是否洗涤干净,可取最后一次洗涤液,先加入___,振荡、静置,再向上层清液中滴加____,观察现象即可判断。
A.硝酸银溶液 B.过量的氯化钡溶液 C.过量的硝酸钡溶液
【答案】Fe2O3+3CO![]() 2Fe+3CO2 漏斗 C 防止碳酸氢铵受热分解 常温下K2SO4的溶解度小(意思相近即可) C C A
2Fe+3CO2 漏斗 C 防止碳酸氢铵受热分解 常温下K2SO4的溶解度小(意思相近即可) C C A
【解析】
根据反应物的性质书写配平反应方程式;根据混合物的状态分析分离的操作;根据流程图及CO的作用分析解答;根据碳酸氢铵的不稳定性分析解答;根据常见离子的检验原理分析解答。
(1)反应物是一氧化碳和氧化铁,生成物是铁和二氧化碳,反应条件是高温,用观察法配平可得:Fe2O3+3CO![]() 2Fe+3CO2,故答案为:Fe2O3+3CO
2Fe+3CO2,故答案为:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(2)把不溶于液体的固体和液体分离方法是过滤,过滤用到的玻璃仪器有:烧杯、玻璃棒、漏斗,故答案为:漏斗;
(3)反应炉中一氧化碳还原氧化铁生成铁和二氧化碳,过量的一氧化碳会随二氧化碳逸出,因此气体B为一氧化碳和二氧化碳的混合气体,通过足量的氢氧化钠溶液后,二氧化碳与氢氧化钠反应生成碳酸钠和水,因此气体C主要成分是一氧化碳,一氧化碳可作为还原剂重复利用,故答案为:C;
(4)因为碳酸氢铵受热分解为氨气、水、二氧化碳,所以反应I的温度一般需控制在35 ℃以下,防止碳酸氢铵受热分解,故答案为:防止碳酸氢铵受热分解;
(5)根据复分解反应发生的条件,反应2中没有不溶物,但常温下硫酸钾的溶解度很小,在生成物中会以沉淀形式出现,所以反应可以发生;SO![]() 和Ag+也会生成白色的硫酸银沉淀,所以需要先检验SO
和Ag+也会生成白色的硫酸银沉淀,所以需要先检验SO![]() ,然后再检验Cl-;检验SO
,然后再检验Cl-;检验SO![]() 应用硝酸钡溶液,检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入过量的硝酸钡溶液以除去SO
应用硝酸钡溶液,检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入过量的硝酸钡溶液以除去SO![]() ,振荡、静置,再向上层清液中滴加硝酸银溶液以检验Cl-,故答案为:常温下K2SO4的溶解度小(意思相近即可);C ;C;A。
,振荡、静置,再向上层清液中滴加硝酸银溶液以检验Cl-,故答案为:常温下K2SO4的溶解度小(意思相近即可);C ;C;A。

 新编小学单元自测题系列答案
新编小学单元自测题系列答案【题目】已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | Ka=1.8×10﹣5 | Ka1=4.3×10﹣7 Ka2=5.6×10﹣11 | Ka=3.0×10﹣8 |
(1)物质的量浓度均为0.1molL﹣1的四种溶液:pH由小到大排列的顺序是_______(用编号填写)
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1molL﹣1 CH3COOH溶液加水稀释过程中,下列表达式的数据变大的是_____(填字母)_______
A. c(H+) B.![]() C. c(H+)c(OH﹣) D.
C. c(H+)c(OH﹣) D. ![]() E.
E. ![]()
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:__________________
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中
c(CH3COO﹣)﹣c(Na+)=________(填准确数值)。
(5)25℃时,将a molL﹣1的醋酸与b molL﹣1氢氧化钠等体积混合,反应后溶液恰好显中性,用a、b表示醋酸的电离平衡常数为____________________________________
(6)标准状况下,将1.12L CO2通入100mL 1molL﹣1的NaOH溶液中,用溶液中微粒的浓度符号完成下列等式: c(OH﹣)=2c(H2CO3)+_________________________
【题目】某温度下2L密闭容器中,3种气体起始状态和平衡状态时的物质的量(n)如下表所示.下列说法正确的是( )
X | Y | W | |
n(起始状态)/mol | 2 | 1 | 0 |
n(平衡状态)/mol | 1 | 0.5 | 1.5 |
A.该温度下,此反应的平衡常数K=6.75
B.若升高温度,W的体积分数减小,则此反应△H>0
C.增大压强,正、逆反应速率均增大,平衡向正反应方向移动
D.该温度下,此反应的平衡常数表达式是 K= ![]()
【题目】下表是几种常用燃料(1mol)完全燃烧时放出的热量:
物质 | 炭粉(C) | 一氧化碳(CO) | 氢气(H2) | 甲烷(CH4) | 乙醇(C2H5OH) |
状态 | 固体 | 气体 | 气体 | 气体 | 液体 |
热量(kJ) | 392.8 | 282.6 | 285.8 | 890.3 | 1367 |
(1)从热量角度分析,目前最适合家庭使用的优质气体燃料是___。
(2)写出管道煤气中的一氧化碳燃烧的热化学方程式___。
(3)充分燃烧1mol表中各种燃料,排放出二氧化碳的量最多的是___。
(4)矿物燃料储量有限,而且在燃烧过程中会产生污染。根据能源多样化的发展战略,我国开发利用的绿色能源有氢能、___等。