题目内容
1.下列叙述中正确的是( )| A. | 同周期元素中,ⅦA族元素的原子半径最大 | |
| B. | ⅥA族元素的原子,其半径越大,越容易得到电子 | |
| C. | 室温时,零族元素的单质都是气体 | |
| D. | 同一周期中,卤族元素的第一电离能最大 |
分析 A.同周期元素中,从左至右原子半径依次减小;
B.ⅥA族元素的原子,其半径越大,越不容易得电子;
C.室温时,0族元素的单质都是气体;
D.同一周期中,从左向右第一电离能增大.
解答 解:A.同周期元素中,从左至右原子半径依次减小,故A错误;
B.ⅥA族元素的原子,其半径越大,越不容易得电子,故B错误;
C.室温时,0族元素的单质都是气体,故C正确;
D.同一周期中,从左向右第一电离能增大,则碱金属元素的第一电离能最小,稀有气体元素的第一电离能最大,故D错误;
故选C.
点评 本题考查元素的性质,注意把握元素在周期表中的位置及元素周期律即可解答,题目难度大.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
16.下列说法中错误的是( )
| A. | 燃烧、酸碱中和反应都是放热反应 | |
| B. | 化学反应必然伴随着能量的变化 | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量 |
6.金属的下列性质和金属晶体结构无关的是( )
| A. | 良好的导电性 | B. | 良好的延展性 | C. | 反应中易失电子 | D. | 良好的导热性 |
10.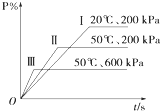 在一密闭容器中进行以下可逆反应:M(g)+P(g)═N(g)+2L.在不同的条件下P的百分含量P%的变化情况如图,则该反应( )
在一密闭容器中进行以下可逆反应:M(g)+P(g)═N(g)+2L.在不同的条件下P的百分含量P%的变化情况如图,则该反应( )
 在一密闭容器中进行以下可逆反应:M(g)+P(g)═N(g)+2L.在不同的条件下P的百分含量P%的变化情况如图,则该反应( )
在一密闭容器中进行以下可逆反应:M(g)+P(g)═N(g)+2L.在不同的条件下P的百分含量P%的变化情况如图,则该反应( )| A. | 正反应放热,L是固体 | B. | 正反应吸热,L是气体 | ||
| C. | 正反应吸热,L是固态 | D. | 正反应放热,L是固体或气体 |
11.下列实验中,溶液颜色不会发生变化的是( )
| A. | SO2通入品红溶液 | B. | 碘酒滴入淀粉溶液 | ||
| C. | 乙烯通入酸性KMnO4溶液中 | D. | Cl2通入NaOH溶液中 |
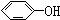 与
与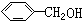
 与
与
 现用邻苯二甲酸氢钾(本题中用KHA表示)标准溶液来测定某NaOH溶液的浓度,进行如下操作:
现用邻苯二甲酸氢钾(本题中用KHA表示)标准溶液来测定某NaOH溶液的浓度,进行如下操作: