题目内容
14.乙二酸( HOOC-COOH)俗称草酸,易溶于水,电离常数K1=5.4×10-2,K2=5.4×10-5,其盐草酸钙和草酸氢钙均为白色不溶物.无色晶体H2C2O4•2H2O称为草酸晶体,其熔点为101.5℃.草酸晶体失去结晶水得无水草酸,它在157℃升华.根据上述信息,回答下列问题.
(1)向盛有2mL饱和NaHCO3溶液的试管里加入少量乙二酸浓溶液,观察到有大量气泡产生,写出该反应的离子方程式:2HCO3-+H2C2O4=2H2O+2CO2↑+C2O42-.(碳酸:K1=4.4×10-7)
(2)向试管A中加入3mL乙醇,然后边振荡试管边加入2mL浓硫酸和2mL乙二酸溶液,按下图Ⅰ组装好装置,加热3-5min.在装有饱和Na2CO3溶液的试管B中有油状且带有香味的液体产生.B中导管口在液面上而不伸入液面下的原因是防止倒吸.写出乙二酸与少量乙醇反应的化学反应方程式
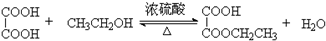 .
.(3)已知草酸分解的化学方程式为:H2C2O4$\stackrel{187℃}{→}$H2O+CO2↑+CO↑
利用图Ⅱ①和图Ⅱ②加热草酸晶体(夹持仪器忽略),以验证草酸受热是否分解.连续加热一段时间后的现象是:图Ⅱ①:试管里澄清石灰水先变浑浊,后又变澄清;
图Ⅱ②:试管里澄清石灰水只变浑浊.
能验证草酸受热分解的装置是①(填图Ⅱ中的编号“①”或“②”).
(4)图Ⅱ①中冷凝管的作用是:冷凝回流草酸蒸气,防止生成草酸盐沉淀对CO2的检出造成干扰.
分析 (1)由电离常数可知,HC2O4-酸性大于碳酸,应生成C2O42-、二氧化碳、水;
(2)乙二酸与少量乙醇反应生成乙二酸乙酯,注意防止倒吸;
(3)如乙二酸分解,则生成二氧化碳气体,可使澄清石灰水变浑浊,但要排出乙二酸钙的影响;
(4)为防止乙二酸的影响,用冷凝管进行分离.
解答 解:(1)由电离常数可知,HC2O4-酸性大于碳酸,应生成C2O42-、二氧化碳、水,反应的离子方程式为2HCO3-+H2C2O4=2H2O+2CO2↑+C2O42-,
故答案为:2HCO3-+H2C2O4=2H2O+2CO2↑+C2O42-;
(2)乙二酸与少量乙醇反应生成乙二酸乙酯,方程式为 ,因生成物含有乙醇,易溶于水,为防止倒吸,则导管口在液面上而不伸入液面下,
,因生成物含有乙醇,易溶于水,为防止倒吸,则导管口在液面上而不伸入液面下,
故答案为:防止倒吸; ;
;
(3)①试管里澄清石灰水先变浑浊,后又变澄清,说明生成二氧化碳,二氧化碳先与氢氧化钙反应生成碳酸钙,碳酸钙与二氧化碳反应生成碳酸氢钙,
故答案为:①;
(4)乙二酸沸点较高,加热时,为防止乙二酸与氢氧化钙反应生成草酸钙对实验现象、结论有影响,则应用冷凝管进行蒸馏分离,
故答案为:冷凝回流草酸蒸气,防止生成草酸盐沉淀对CO2的检出造成干扰.
点评 本题考查性质实验的探究,侧重于学生的分析、实验能力的考查,注意把握实验的原理、目的和操作方法,题目难度中等.

练习册系列答案
相关题目
4.下列有关说法正确的是( )
| A. | CaCO3(s)═CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 | |
| B. | 镀锌铁皮镀层受损后,铁比受损前更容易生锈 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,反应速率V(H2)增大 | |
| D. | 一定条件下水由气态变为液态是熵增加的过程 |
5.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 13.8 g N02与足量水反应,转移电子数目为0.2 NA | |
| B. | 标准状况下,22.4 L溴苯中含有氢原子数目为5NA | |
| C. | 500 mL 2 mol/L NH4N03溶液中,含有NH4+数目为NA | |
| D. | 用惰性电极电解足量CuS04溶液,生成22.4 L气体时转移电子数目为4 NA |
19.下列有关离子方程式书写正确的( )
| A. | 向含1molFeI2溶液中通入标准状况下22.4LCl22Fe2++2I-+2Cl2=2Fe3++I2+2Cl- | |
| B. | 在Na2S溶液中滴加少量FeCl3 2Fe3++S2-═2Fe2++S↓ | |
| C. | 氯化铝溶液中加入过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O=C6H5OH+HSO${\;}_{3}^{-}$ |
6.亚氨基锂(Li2NH)是一种储氢容量高、安全性好的固体储氢材料,其储氢原理可表示为:Li2NH+H2═LiNH2+LiH下列说法正确的是( )
| A. | 亚氨基锂(Li2NH)中N的化合价为-1 | |
| B. | 此法储氢和钢瓶储氢的原理相同 | |
| C. | Li+和H-的半径相同 | |
| D. | 该反应中氢气既是氧化剂又是还原剂 |
3.下列有关化学用语或说法正确的是( )
| A. | 硫原子的原子结构示意图: | |
| B. | NH4Cl的电子式: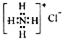 | |
| C. | ${\;}_{62}^{144}$Sm与${\;}_{62}^{150}$Sm为不同的核素,有不同的化学性质 | |
| D. | 在固态水中,水分子间以氢键结合成排列规整的晶体,在这种晶体中有空隙,造成体积膨胀,密度减小至低于水的密度 |
 .
.