题目内容
17.四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍.| X | Y | |
| Z | W |
(1)元素Z位于周期表中的位置第三周期VA族;
(2)这些元素的氢化物中,水溶液碱性最强的是NH3(写化学式);
(3)XW2的电子式为
 ;
;(4)Y的最高价氧化物的化学式为N2O5;
(5)W和Y形成的一种二元化合物具有色温效应,其相对分子质量在170~190之间,且W的质量分数约为70%.该化合物的化学式为S4N4.
分析 X、Y、Z、W均为短周期元素,由位置关系可知,X、Y处于第二周期,Z、W处于第三周期,Z元素原子核外电子总数是其最外层电子数的3倍,设核外最外层电子数为x,则有(2+8+x)=3x,解得x=5,则Z为P元素,故X为C元素、Y为N元素、W为S元素,据此解答.
解答 解:X、Y、Z、W均为短周期元素,由位置关系可知,X、Y处于第二周期,Z、W处于第三周期,Z元素原子核外电子总数是其最外层电子数的3倍,设核外最外层电子数为x,则有(2+8+x)=3x,解得x=5,则Z为P元素,故X为C元素、Y为N元素、W为S元素.
(1)元素Z为磷元素,位于周期表中的位置:第三周期VA族,故答案为:第三周期VA族;
(2)这些元素的氢化物中,NH3的水溶液碱性最强,故答案为:NH3;
(3)CS2的电子式为 ,故答案为:
,故答案为: ;
;
(4)Y为N元素,最高价氧化物的化学式为N2O5,故答案为:N2O5;
(5)Y为N元素,W为S元素,形成的化合物中S的质量分数为70%,则S和N原子个数比为$\frac{70%}{32}$:$\frac{1-70%}{14}$=1:1,其相对分子质量在170~190之间,设化学式为(SN)x,则170<46x<190,解得x=4时,故二者形成的分子式为S4N4,故答案为:S4N4.
点评 本题考查元素周期表与元素周期律、无机物推断、常用化学用语等,难度中等,注意对元素周期律的理解掌握.

练习册系列答案
相关题目
7.丙烯酸(CH2=CH-COOH)的性质可能有( )
①取代反应;②加成反应;③氧化反应;④酯化反应;⑤水解反应.
①取代反应;②加成反应;③氧化反应;④酯化反应;⑤水解反应.
| A. | ①、②、③、④ | B. | ②、③、④、⑤ | C. | ①、②、④、⑤ | D. | 全部 |
8.下列符号中能表示宏观意义的有( )
| A. | 2Cl2 | B. | 3SO2 | C. | N2 | D. | 3Na |
12.下列各物质中所含分子个数由大小的顺序正确的是( )
①0.6molNH3;②标准状况下22.4L氦气;③4℃时9mL水;④0.2molH3PO4.
①0.6molNH3;②标准状况下22.4L氦气;③4℃时9mL水;④0.2molH3PO4.
| A. | ①④③② | B. | ④③②① | C. | ②①③④ | D. | ①④②③ |
2.用来检验Fe3+是否存在的最佳试剂是( )
| A. | H2S | B. | NaOH | C. | Na2CO3 | D. | KSCN |
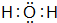 .
.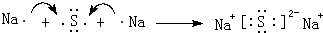 .
.