题目内容
【题目】我国科学家设计了一种太阳能驱动的H2S分解装置,工作原理如图所示。下列叙述正确的是( )

A.甲区发生反应的离子方程式为:2Fe3++S2-=2Fe2++S↓
B.理论上每生成1molS时,H+由质子交换膜右侧向左侧移动的物质的量为2mol
C.丙区发生的电极反应为:H4[SiW12O40]+2e-+2H+=H6[SiW12O40]
D.丁区H6[SiW12O40]在催化剂表面发生电化学反应生成H4[SiW12O40]和H2
【答案】C
【解析】
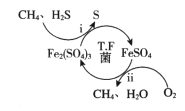
根据图可知,甲区:通入H2S,发生:H2S+2Fe3+=2Fe2++S↓+2H+,S通过甲装置下端排出,Fe2+与H+通过甲乙之间的泵到达乙区,Fe2+在乙区失去电子,发生:Fe2+-e-= Fe3+,Fe3+从左上面管子到甲区循环,H+通过质子交换膜进入丙区,发生:H4[SiW12O40]+2e-+2H+=H6[SiW12O40],H6[SiW12O40]从右上管到达丁区,在催化剂作用下发生:H6[SiW12O40]= H4[SiW12O40]+H2↑,H4[SiW12O40]从丙丁之间的泵回到丙区循环,H2排出,据此分析解答。
A. 甲区:通入H2S,发生的离子反应方程式为:H2S+2Fe3+=2Fe2++S↓+2H+,A错误;
B. H+由质子交换膜左侧向右侧移动,B错误;
C. 丙区:发生反应为:H4[SiW12O40]+2e-+2H+=H6[SiW12O40],C正确;
D. 丁区:在催化剂作用下发生:H6[SiW12O40]= H4[SiW12O40]+H2↑,没发生电化学反应,D错误;故答案为:C。

【题目】I.已知,常温下H2S、H2CO3的电离常数如表
Ka1 | Ka2 | |
H2S | 9.1×10-8 | 1×10-15 |
H2CO3 | 4.3×10-7 | 5.6×10-11 |
(1)①常温下,0.1 mol·L-1的硫化钠溶液和0.1mol·L-1的碳酸钠溶液,碱性更强的是_______。其原因是_____________________________。
②常温下,硫化钠水解的离子方程式为_____________________________。
(2)常温下,向100mL0.1mol·L-1H2S溶液中滴加0.1mol·L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
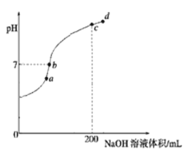
试分析图中a、b、c、d四个点,水的电离程度最大的是________。
II.减少NO2、SO2、CO等有害气体对大气环境的危害,是人类的共同追求。
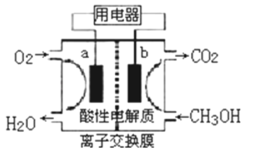
(3)以甲醇做燃料的电池,如图所示,其负极反应式为________,该燃料电池在理想状态下,将有96.5%的化学能转化成电能,即消耗1mol液体甲醇所能产生的最大电能达702.1kJ,则通常甲醇燃烧的热化学反应方程式为________。
(4)已知:NO2(g)+SO2(g)![]() SO3(g)+NO(g) △H=+41.8kJmol﹣1。一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的________。
SO3(g)+NO(g) △H=+41.8kJmol﹣1。一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的________。
a.体系压强保持不变 b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变 d.每消耗1molSO3的同时生成1molNO2
(5)当上述反应平衡时,测得NO2与SO2体积比为1:6,则平衡常数K=________。