题目内容
下列元素中基态原子的第一电离能最大的是( )
| A.B | B.C | C.N | D.O |
C
解析试题分析:非金属性越强,第一电离能越大。但由于氮元素的2p轨道电子处于半充满状态,稳定性强,因此氮元素的第一电离能大于氧元素的第一电离能,答案选C。
考点:考查第一电离能的大小比较
点评:该题是高考中的常见题型和考点,试题紧扣教材,基础性强,难度不大。明确第一电离能的含义、判断依据是答题的关键。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列提出原子学说的科学家是( )
| A.拉瓦锡 | B.道尔顿 | C.门捷列夫 | D.波义耳 |
元素周期表和元素周期律可以指导人们进行规律性的推测和判断。下列说法不合理的是
| A.若X+和Y2-的核外电子层结构相同,则原子序数:X > Y |
| B.由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S |
| C.硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
| D.Cs和Ba分别位于第六周期IA和IIA族,碱性:CsOH >Ba(OH)2 |
下列各组粒子所含电子数目相同的是
| A.NH4+、OH-、H3O+ |
| B.Na+、Mg2+、S2- |
| C.F-、NH2-、Cl- |
| D.Li+、Na+、K+ |
下列排列顺序不正确的是
| A.热稳定性:CH4> SiH4 >HF | B.原子半径:Na>Mg>O |
| C.酸性:HClO4>H2SO4>H3PO4 | D.非金属性:F>Cl>Br |
下列分子中所有原子都满足最外层为8电子结构的是( )
| A.CS2 | B.PCl5 | C.HClO | D.BeCl2 |
(4分)下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
| | | | |||||
| | | | a | | | | |
| | b | | c | | | d | |
(1)元素b的基态原子电子排布式为 。
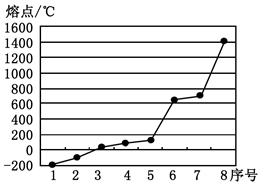
(2)第三周期8种元素按单质熔点高低的排列顺序如右图,其中序号“8”代表 (填元素符号);其中电负性最大的是 (填右图中的序号)。
(3)元素a、c分别与元素d形成的化合物中,熔点较高的是(填化学式)。
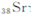 )元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与
)元素广泛存在于矿泉水中,是一种人体必需的微量元素,在元素周期表中与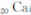
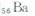 同属于第ⅡA族?
同属于第ⅡA族?