题目内容
【题目】如何降低大气中![]() 的含量及有效地开发利用
的含量及有效地开发利用![]() 引起了全世界的普遍重视。目前工业上有一种方法是用
引起了全世界的普遍重视。目前工业上有一种方法是用![]() 来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入
来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入![]() 和
和![]() ,在
,在![]() 下发生发应
下发生发应![]() 实验测得
实验测得![]() 和
和![]() 的物质的量
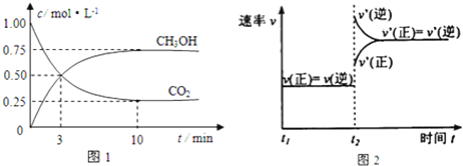
的物质的量![]() 随时间变化如图1所示:
随时间变化如图1所示:
(1)下列事实能说明反应到达平衡状态的是______________
A.容器内的密度不再改变 B. CO2和H2 的物质的量比不再改变
C.v正(CO2)=3v逆(H2) D. 容器内的压强不再改变
(2)![]() 达平衡时,
达平衡时,![]() 的体积分数为____________,平衡常数为______
的体积分数为____________,平衡常数为______![]() 保留两位小数
保留两位小数![]() ;该温度下,测得某时刻,
;该温度下,测得某时刻,![]() 、
、![]() 、
、![]() 和
和![]() 的浓度均
的浓度均![]() ,则此 时
,则此 时![]() 正
正![]() ______
______![]() 逆
逆![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() 。
。
(3)由图2可知,当温度升高到![]() 达平衡时,K值__________
达平衡时,K值__________![]() 填“增大”“减小”或“不变”
填“增大”“减小”或“不变”![]() 。
。
(4)下列措施中不能使![]() 的转化率增大的是______。
的转化率增大的是______。
A.在原容器中再充入1mol![]()
B.在原容器中再充入![]()
C.缩小容器的容积
![]() 使用更有效的催化剂
使用更有效的催化剂
E.将水蒸气从体系中分离出
F.在原容器中充入1molHe
【答案】D ![]() 5.33 > 减小 BDF
5.33 > 减小 BDF
【解析】
⑴中A选项,根据密度公式![]() ,气体质量没有变化,容器体积没有变化,即密度始终没有改变,因此不能作为判断平衡的标志,故A错误;
,气体质量没有变化,容器体积没有变化,即密度始终没有改变,因此不能作为判断平衡的标志,故A错误;
B选项,CO2和H2开始比是1:3,在整个反应过程中消耗也是按照1:3在消耗,因此在反应过程中剩余的CO2和H2的物质的量比始终未1:3,因此不能作为判断平衡的标志,故B错误;
C选项,v正(CO2),反应正方向,v逆(H2),反应逆方向,两个不同的方向,还要遵循速率比等于计量系数之比,应该3v正(CO2) = v逆(H2),故C错误;
D选项,该反应为不等体积反应,因此正向反应时,容器内的压强在不断减小,当压强不再改变时就达到平衡,故D正确;
综上所述,答案D。
⑵根据反应及图像分析,利用“三步走”思想
CO2(g) + 3H2(g) ![]() CH3OH (g) + H2O(g)
CH3OH (g) + H2O(g)
开始 1 mol·L-1 3 mol·L-1 0 0
转化 0.75 mol·L-1 2.25 mol·L-1 0.75 mol·L-1 0.75 mol·L-1
平衡 0.25 mol·L-1 0.75 mol·L-1 0.75 mol·L-1 0.75 mol·L-1
![]()
故第一空答案为30%;
根据平衡常数公式代入
![]()
故第二空答案为5.33;
根据浓度商公式代入得出数据与化学平衡常数比较
![]()
浓度商小于平衡常数,即要变大,则生成物要增加,平衡正向移动即正反应速率大于逆反应速率,故第三空答案为“>”;
⑶根据图象知,升高温度,逆反应速率大于正反应速率,平衡向逆反应方向移动,K值减小,故答案为减小;
⑷A选项,在原容器中再充入1mol氢气,平衡向正反应方向移动,二氧化碳消耗,二氧化碳的转化率增大,故A能增大转化率;
B选项,在原容器中再充入1 mol 二氧化碳,平衡正向移动,虽然二氧化碳又消耗了,根据转化率公式可知,分子分母都变大,由于平衡移动是微弱的,因此分子增加幅度小于分母增加的幅度,转化率减小,故B不能增大转化率;
C选项,缩小容器的容积,压强增大,平衡向体积减小的方向移动即正向移动,转化率变大,故C能增大转化率;
D选项,使用更有效的催化剂,反应速率加快,但平衡没有发生移动,转化率不变,故D不能增大转化率;
E选项,将水蒸气从体系中分离出即减小生成物浓度,平衡正向移动,转化率增大,故E能增大转化率;
F选项,在原容器中充入1molHe,体系压强增大,但反应浓度没有发生改变,平衡不移动,转化率不变;故F不能增大转化率;
综上所述,正确答案为BDF

【题目】下表给出七种元素的相关信息,根据以下信息填空:
元素 | 相关信息 |
A | 核外电子数和电子层数相等 |
B | 基态原子2p能级有3个未成对电子 |
C | 在地壳中含量最高 |
D | 目前,在元素周期表中电负性最大 |
E | 基态原子核外电子分处6个不同能级,且每个能级均已排满 |
F | 原子序数等于D与E的原子序数之和 |
G | 基态原子2p能级上有两个空轨道 |
(1)写出D在元素周期表中的位置___________________。
(2)14gB的单质分子中π键的个数为____________。
(3)C元素的氢化物的沸点是同族元素氢化物中最高的,原因是________。
(4)B、C、D 3种元素的电负性由大到小的顺序为________(用元素符号表示)。
(5)写出一种与B2互为等电子体的分子或离子____________。
(6)已知BA5为离子化合物,写出其电子式:_______。
(7)第二周期中,第一电离能介于B元素和G 元素间的元素为 ____(填“元素符号”)。