题目内容
【题目】根据电化学知识回答下列问题。
Ⅰ、某小组同学设想用如图装置电解硫酸钾溶液来制取氧气、氢气、硫酸和氢氧化钾。
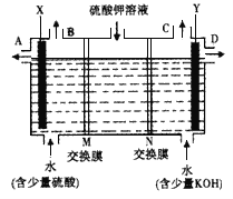
(1)X极与电源的_____(填正或负)极相连,氢气从____ (选填A、 B、C或D)口导出。
(2)离子交换膜只允许一类离子通过,则M为________(填阴离子或阳离子,下同)交换膜,N为________交换膜。
(3)若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃料电池(石墨为电极),则电池正极的电极反应式为___________________
Ⅱ、铅蓄电池是常见的二次电池,其放电反应和充电反应表示如下:Pb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(l)
2PbSO4(s)+2H2O(l)
写出它放电时正极的电极反应式______________________________________;
充电时阴极的电极反应式______________________________________________。
【答案】正 C 阴离子 阳离子 O2+2H2O+4e-=4OH- PbO2+4H++SO42-+2e-=PbSO4+2H2O PbSO4 + 2e- = Pb + SO42-
【解析】
Ⅰ(1)根据加入的物质可知,X电极附近生成硫酸,Y电极附近生成氢氧化钾去分析阴阳极;
(2)电解过程中,电解质溶液中阳离子向阴极移动,阴离子向阳极移动;
(3)原电池中正极上得电子发生还原反应;
Ⅱ 由铅蓄电池的总反应PPb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(l)可知,放电时,Pb被氧化,应为电池负极反应,电极反应式为Pb-2e-+SO42-=PbSO4,正极上PbO2得电子被还原,电极反应式为PbO2+SO42-+2e-+4H+=PbSO4+2H2O,在充电时,阳极上发生氧化反应,电极反应式和放电时的正极反应互为逆反应,阴极上发生还原反应,电极反应式和放电时的负极反应互为逆反应,以此解答该题。
2PbSO4(s)+2H2O(l)可知,放电时,Pb被氧化,应为电池负极反应,电极反应式为Pb-2e-+SO42-=PbSO4,正极上PbO2得电子被还原,电极反应式为PbO2+SO42-+2e-+4H+=PbSO4+2H2O,在充电时,阳极上发生氧化反应,电极反应式和放电时的正极反应互为逆反应,阴极上发生还原反应,电极反应式和放电时的负极反应互为逆反应,以此解答该题。
Ⅰ(1)题图中左边加入含硫酸的水,右侧加入含KOH的水,说明左边制硫酸,右边制备KOH溶液,氢氧根离子在阳极放电,同时电解后溶液呈酸性,氢离子在阴极放电,同时电解后溶液呈碱性,则X为阳极,Y为阴极,所以X连接电源正极;Y电极上氢离子放电生成氢气,所以氢气从C口导出;
答案:正;C;
(2)OH-在阳极发生氧化反应,使左边溶液中H+增多,为了使溶液呈电中性,硫酸钾溶液中的SO42-通过M交换膜向左边迁移,即M为阴离子交换膜;H+在Y极发生还原反应,使右边溶液中OH-增多,硫酸钾溶液中K+向右迁移,N为阳离子交换膜;
答案:阴离子;阳离子;
(3)氢氧燃料碱性电池中,通入氧气的电极是正极,正极上氧气得电子发生还原反应,电极反应式为O2+2H2O+4e-=4OH-;
答案:O2+2H2O+4e-=4OH-
Ⅱ 由铅蓄电池的总反应PPb(s)+PbO2(s)+2H2SO4(aq)![]() 2PbSO4(s)+2H2O(l)可知,放电时,Pb被氧化,应为电池负极反应,电极反应式为Pb-2e-+SO42-=PbSO4,正极上PbO2得电子被还原,电极反应式为PbO2+SO42-+2e-+4H+=PbSO4+2H2O,在充电时,阳极上发生氧化反应,电极反应式和放电时的正极反应互为逆反应,阴极上发生还原反应,电极反应式和放电时的负极反应互为逆反应;
2PbSO4(s)+2H2O(l)可知,放电时,Pb被氧化,应为电池负极反应,电极反应式为Pb-2e-+SO42-=PbSO4,正极上PbO2得电子被还原,电极反应式为PbO2+SO42-+2e-+4H+=PbSO4+2H2O,在充电时,阳极上发生氧化反应,电极反应式和放电时的正极反应互为逆反应,阴极上发生还原反应,电极反应式和放电时的负极反应互为逆反应;
答案:PbO2+4H++SO42-+2e-=PbSO4+2H2O PbSO4 + 2e- = Pb + SO42-

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案