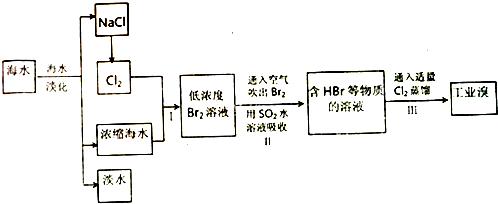
题目内容
15.下列分值中,所有原子的最外层均满足8电子稳定结构的是( )| A. | PCl5 | B. | N2 | C. | BF3 | D. | H2O |
分析 化合物分子中某原子最外层电子数=元素原子最外层电子数+该元素原子化合价绝对值,若该值等于8,则该原子满足8电子结构;而单质分子中根据原子的最外层电子式与形成的共用电子对数判断.
解答 解:A.PCl5中Cl元素化合价为-1,Cl原子最外层电子数是7,1+7=8,P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,分子中P原子不满足8电子结构,故A错误;
B.N原子最外层电子数是5,N2中两个N原子之间存在3个共用电子对,则N2中N原子的最外层电子式为5+3=8,所以满足8电子结构,故B正确;
C.BF3中F元素化合价为-1,F原子最外层电子数是7,1+7=8,B元素化合价为+3,B原子最外层电子数为3,所以3+3=6,分子中B原子不满足8电子结构,故C错误;
D.H2O中H原子的最外层电子数为2,则分子中H原子不满足8电子结构,故D错误;
故选B.
点评 本题考查了8电子结构判断,注意分子中含有氢元素,该分子一定不满足各原子达8电子结构,题目难度不大.

练习册系列答案
相关题目
6.下列有关物质的用途错误的是( )
| A. | 水玻璃可用作木材防火剂 | B. | 二氧化硅是制造光导纤维的材料 | ||
| C. | 可用氢氟酸刻蚀玻璃 | D. | 石英是制造太阳能电池的常用材料 |
3.化学家借助太阳能产生的电能和热能,用空气和水作原料合成了氨气.下列有关说法正确的是( )
| A. | 该合成中所有的电能和热能全部转化为化学能 | |
| B. | 该合成氨过程不属于氮的固定 | |
| C. | 空气、水、太阳能均为可再生资源 | |
| D. | 断裂N2中的N≡N键会释放出能量 |
10.下列叙述正确的是( )
| A. | 第三周期元素形成的简单离子中半径最小的是Na+ | |
| B. | 同周期元素(过渡元素和0族元素除外)从左到右,原子半径逐渐减小 | |
| C. | 带ⅦA族元素从上到小,其氢化物的稳定性逐渐增强 | |
| D. | 同主族元素从上到下,单质的熔点逐渐降低 |
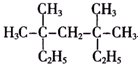 3,3,5,5-四甲基庚烷.
3,3,5,5-四甲基庚烷. .
. .
.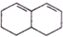 与Br2发生1,4-加成反应的化学方程式为
与Br2发生1,4-加成反应的化学方程式为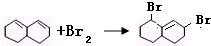 .
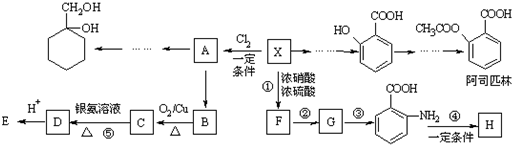
.
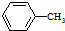 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$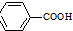
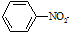 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$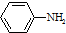 (苯胺,易被氧化)
(苯胺,易被氧化)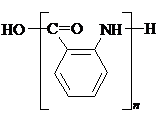 或
或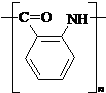 ;
;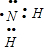 ;
;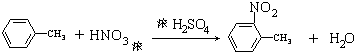 ;
;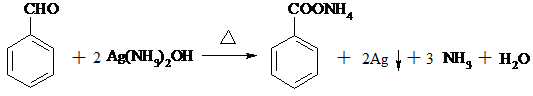 ;
;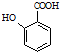 有多种同分异构体,写出2种含有1个醛基和2个羟基的芳香族化合物的结构简式:
有多种同分异构体,写出2种含有1个醛基和2个羟基的芳香族化合物的结构简式: ;
;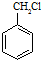 和其他无机物合成
和其他无机物合成 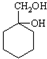 最合理的方案(不超过4步).
最合理的方案(不超过4步).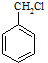 $→_{反应条件}^{反应物}$…$→_{反应条件}^{反应物}$
$→_{反应条件}^{反应物}$…$→_{反应条件}^{反应物}$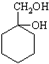
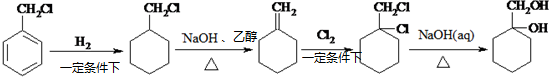 .
.