题目内容
已知H2(g)+Br2(g)→2HBr(g)+72kJ.1mol Br2(g)液化放出的能量为30kJ,其它相关数据如下表:
则上述表格中的a值为( )
| H2(g) | Br2(l) | HBr(g) | |
| 1mol 分子中的化学键断裂时需要吸收的能量/kJ | 436 | a | 369 |
| A、404 | B、344 |
| C、260 | D、200 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:根据盖斯定律计算反应H2(g)+Br2(g)=2HBr(g)的△H,结合反应热等于反应物的总键能减生成物的总键能列方程计算.
解答:
解:在H2(g)+Br2(l)=2HBr(g)△H=-42kJ/mol反应中,1mol Br2(g)液化放出的能量为30kJ,即Br2(g)=Br2(l)△H=-30kJ/mol,则H2(g)+Br2(g)=2HBr(g)△H=-72kJ/mol,反应热等于反应物的总键能减生成物的总键能,则-72=436+a-2×369,a=230,
故选:C.
故选:C.
点评:本题考查反应热的计算,题目难度不大,注意反应热与键能的计算关系以及物质的不同聚集状态的转化.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
下列元素中,金属性最强的是( )
| A、K | B、Al | C、He | D、S |
钛被称为21世纪金属,是研制卫星、火箭、宇宙飞船及深海潜艇的重要材料.研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置模拟获得金属钙(需定期更换石墨棒),并以钙为还原剂,还原二氧化钛制备金属钛.下列叙述正确的是( )
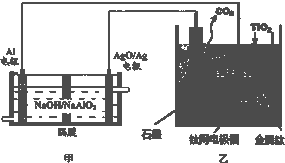

| A、甲装置工作过程中OH-向AgO/Ag极移动;乙装置工作过程中O2-向阴极移动 | ||
| B、乙装置阳极的电极反应式为C+2O2--4e-═CO2↑ | ||
C、若电解金属钛效率为η,则获取1mol Ti时消耗Al的物质的量
| ||
| D、在制备金属钛前后,整套装置中CaO的总量减少 |
下列说法正确的是( )
| A、NaCl和SiC晶体熔化时,克服微粒间作用力的类型相同 |
| B、24Mg32S晶体中电子总数与中子总数之比为1:1 |
| C、用乙醇或CCl4可提取碘水中的碘单质 |
| D、H2S和SiF4分子中各原子最外层都满足8电子结构 |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,0.56L丙烷中含有共价键的数目为0.2NA |
| B、0.1mol H2O和D2O组成的混合物中含有的中子数是NA |
| C、标准状况下,2.24L Cl2溶于水,转移的电子数目为0.1NA |
| D、常温下,20L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA |
白磷和红磷燃烧的产物都是P2O5,但是相同条件下等量的白磷和红磷燃烧前者放出热量多.以下说法正确的是( )
| A、红磷比白磷稳定 |
| B、白磷转化成红磷吸收热量 |
| C、红磷转化成白磷为放热反应 |
| D、等量的白磷和红磷相互转化时的能量变化值不相等 |
 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.