题目内容
2.下列各组微粒中,核外电子总数相等的是( )| A. | Na+和Li+ | B. | CO和CO2 | C. | H2O 和Al3+ | D. | NO和CO |
分析 在原子中,核内质子数等于核外电子数,分子是由原子构成的,所以分子的电子总数就等于构成分子的各原子的电子数之和.金属离子的核外电子数等于原子的核外电子数减电荷数.
解答 解:A、钠原子有11个电子,Na+核外电子总数为10,锂原子有3个电子,Li+核外电子总数为2,故A错误.
B、碳原子有6个电子,氧原子有8个电子,CO中核外电子总数是14,碳原子有6个电子,氧原子有8个电子,CO2中核外电子总数是22,故B错误;
C、氢原子有1个电子,氧原子有8个电子,H2O 中核外电子总数是10,铝原子有13个电子,Al3+核外电子总数为10,故C正确;
D、氮原子的有7个电子,氧原子有8个电子,NO核外电子总数是15,碳原子有6个电子,氧原子有8个电子,CO中核外电子总数是14,故D错误;
故选:C.
点评 本题考查了分子中电子总数的计算,题目难度不大,注意计算分子的电子总数就等于构成分子的各原子的电子数之和.

练习册系列答案
相关题目
12.同族元素所形成的同一类型的化合物,其结构和性质往往相似.化合物PH4I是一种白色晶体,跟NH4Cl的性质相似,则下列对它的描述中正确的是( )
| A. | 它是一种共价化合物 | |
| B. | 在加热时此化合物最终分解为PH3和HI | |
| C. | 这种化合物不能跟碱反应 | |
| D. | 该化合物可以由PH3和HI化合而成 |
13.日本核事故释放出的极微量人工放射性核素131I,它能引发甲状腺癌;但127I却是人体必需的.127I可阻隔甲状腺吸收放射性131I.碘盐含127I为 30mg•kg-1,成人一次摄入碘盐约3kg才有预防效果. 下列有关说法不正确的是( )
| A. | 131I与127I互为同位素 | |
| B. | 相同物质的量的131I与127I的质子数不同 | |
| C. | 131I与127I 是两种不同核素 | |
| D. | 日用碘盐对预防碘辐射起不到有效作用 |
10.CH3OH和C2H5OH的混合物与浓H2SO4共热,可能生成的有机物最多有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
7.下列实验中,不能观察到明显的变化的是( )
| A. | 把氯气通入FeCl2溶液中 | |
| B. | 把绿豆大的钾投入水中 | |
| C. | 把一段打磨过的镁带放入少量冷水中 | |
| D. | 把溴水滴加到KI淀粉溶液中 |
14.下列对于反应3NO2+H2O=2HNO3+NO的说法中正确的是( )
| A. | 氧化剂与还原剂的质量比为1:2 | |
| B. | NO2是氧化剂水是还原剂 | |
| C. | 生成1molNO则有6mol电子发生转移 | |
| D. | 氧化剂与还原剂的物质的量比为2:1 |
11.X、Y、Z是短周期元素,已知X元素的原子核内无中子,Y元素的最高正价与负价代数和为2,Z元素原子的最外层达到相对稳定结构所需电子数恰好等于其内层电子数,则X、Y、Z三种元素所形成化合物的化学式表示错误的是( )
| A. | XYZ2 | B. | XYZ3 | C. | X2YZ3 | D. | X3YZ4 |
12.下列叙述正确的是( )
| A. | 发生化学反应时失去电子越多的金属原子,还原能力越强 | |
| B. | 金属阳离子被还原后,一定得到该元素的单质 | |
| C. | 核外电子总数相同的原子,一定是同种元素的原子 | |
| D. | 化合反应和置换反应均属于氧化还原反应 |
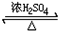 CH3COOC2H5+H2O反应类型取代反应;
CH3COOC2H5+H2O反应类型取代反应; 反应类型加聚反应.
反应类型加聚反应.