题目内容
已知N2O4(g)?2NO2(g) △H>0且平衡体系的总质量(m总 )与总物质的量(n总)之比在不同温度下随压强变化曲线如图所示,下列说法正确的是( )
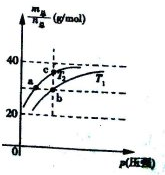

| A.平衡常数K(a)=K(b)<K(c) |
| B.反应速率:va<vb; |
| C.温度:T2>T1 |
D.当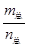 =69g/mol时,若n(NO2):n(N2O4)=2:1, =69g/mol时,若n(NO2):n(N2O4)=2:1, |
B
试题分析:反应N2O4(g)?2NO2(g) △H>0的正反应是吸热反应,在压强不变时,升高温度,平衡正向移动,气体的物质的量增大,平衡体系的总质量(m总 )与总物质的量(n总)之比减小。因此温度: T1 > T2。C 错误。化学平衡常数只与温度有关,而与压强无关。由于a、c在温度T2线上,b在温度T1线上。升高温度化学平衡正向移动,化学平衡常数增大,所以K(a)=" K(c)" < K(b)。A错误。由于b点的温度比a点高,压强比a点大,升高温度,化学反应速率加快;增大压强,化学反应速率加快,故化学反应速率va<vb。B正确。D.若n(NO2):n(N2O4)=2:1,则m总 :n总=(46×2g+92g)÷3mol=61.33g/mol<69g/mol。错误。

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
 (正反应放热)。测得n(O2)随时间的变化如下表
(正反应放热)。测得n(O2)随时间的变化如下表
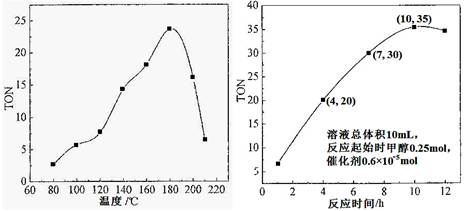
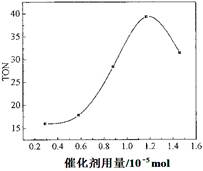
 2NH3,2 min后测得容器中生成了1mol NH3,试求:
2NH3,2 min后测得容器中生成了1mol NH3,试求: 2C(g),?H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500 ℃时充分反应达平衡后C的浓度为ω mol/L,放出热量为b kJ。
2C(g),?H=-a kJ/mol(a>0),在一个有催化剂的固定容积的容器中加入2 mol A和1 mol B,在500 ℃时充分反应达平衡后C的浓度为ω mol/L,放出热量为b kJ。 2C(g)+2D(g),在不同条件下的化学反应速率,其中反应速率最快的是( )
2C(g)+2D(g),在不同条件下的化学反应速率,其中反应速率最快的是( )


 2Z
2Z 2NH3(g),△H=-92.4 kJ.mol-1下列叙
2NH3(g),△H=-92.4 kJ.mol-1下列叙