题目内容
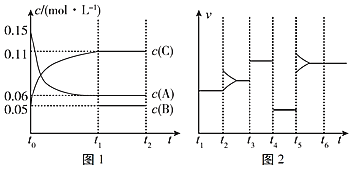
【题目】一定条件下向某密闭容器中加入0.3mol A、0.1mol C和一定量的B三种气体,图1表示各物质浓度随时间的变化关系,图2表示速率随时间的变化关系,t2、t3、t4、t5时刻各改变一种条件,且改变的条件均不同。若t4时刻改变的条件是压强,则下列说法错误的是( )
A.若t1=15s,则前15s的平均反应速率υ(C)=0.004molL﹣1s﹣1
B.该反应的化学方程式为3A![]() B+2C
B+2C
C.t2、t3、t5时刻改变的条件可能分别是增大反应物浓度、加入催化剂、升高温度
D.若t1=15s,则B的起始物质的量为0.02mol
【答案】D
【解析】
t4时改变的条件为减小压强,说明反应前后气体的体积相等,t5时正逆反应速率都增大,应是升高温度,t2时正、逆反应速率中只有其中一个增大,应是改变某一物质的浓度,由图甲可知,t1时到达平衡,△c(A)=0.09mol/L,△c(C)=0.06mol/L,二者化学计量数之比为0.09:0.06=3:2,则B为生成物,反应方程式为3A(g)![]() B(g)+2C(g),结合浓度的变化解答该题。
B(g)+2C(g),结合浓度的变化解答该题。
A. 若t1=15s,生成物C在t0t1时间段的平均反应速率为:v=![]() =0.004 molL﹣1s﹣1, A项正确,不符合题意;
=0.004 molL﹣1s﹣1, A项正确,不符合题意;
B. 由以上分析可知反应的化学方程式为:3A(g)![]() B(g)+2C(g),B项正确,不符合题意;
B(g)+2C(g),B项正确,不符合题意;
C. t2时刻该变外界条件,其中某方向速率一瞬间不发生变化,另一方向化学反应速率增大,故t2时刻该变的外加条件为增大反应物浓度,t3时刻该变外界条件,化学反应速率均增大,且正逆化学反应速率相等,故t3时刻该变的外界条件为加入催化剂或压缩体积加压或充入适量A、B、C,t5时刻后正逆化学反应速率均增大,其该变外界条件可能为升温、充入相关参加反应的物质,C项正确,不符合题意;
D. 该反应的方程式为3A(g)![]() B(g)+2C(g),根据方程式可知消耗0.09mol/L的A,则生成0.03mol/L的B,容器的体积为2L,生成B的物质的量为0.06mol,平衡时B的物质的量为0.1mol,所以起始时B的物质的量为0.1mol0.06mol=0.04mol,D项错误,符合题意;
B(g)+2C(g),根据方程式可知消耗0.09mol/L的A,则生成0.03mol/L的B,容器的体积为2L,生成B的物质的量为0.06mol,平衡时B的物质的量为0.1mol,所以起始时B的物质的量为0.1mol0.06mol=0.04mol,D项错误,符合题意;
答案选D。

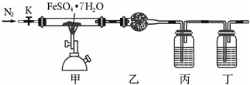
【题目】FeSO4·7H2O广泛用于医药和工业领域,实验室制备FeSO4·7H2O的流程如下:

(1)铁屑与稀硫酸反应前,应用10% Na2CO3溶液浸泡几分钟,操作目的是_________。
(2)最后得到的绿矾晶体用少量冰水洗涤,其目的:①除去晶体表面附着的硫酸等杂质;②_____________________。
(3)FeSO4·7H2O是某些补血剂的主要成分,将1.5 g某补血剂预处理,配成100mL溶液。实验室用KMnO4溶液通过氧化还原滴定测定该补血剂(1.5 g)中铁元素的含量,①配制100 mL 1.200 × 10—2 mol·L—1的KMnO4溶液时,将溶解后的溶液转移至容量瓶中的操作方法是__________________________;
②实验中的KMnO4溶液需要酸化,可用于酸化的酸是_________________。
a. 稀硝酸 b.稀盐酸 c.稀硫酸 d.浓硝酸
KMnO4溶液应盛装在__________滴定管中。滴定到终点时的现象为____________。
③滴定完毕,三次实验记录KMnO4标准溶液的读数如下。
滴定次数实验数据 | 1 | 2 | 3 |
V(样品)/mL | 20.00 | 20.00 | 20.00 |
V(KMnO4)/mL(初读数) | 0.00 | 0.20 | 0.00 |
V(KMnO4)/mL(终读数) | 15.85 | 15.22 | 14.98 |
该补血剂中铁元素的质量分数为_____________________。