题目内容
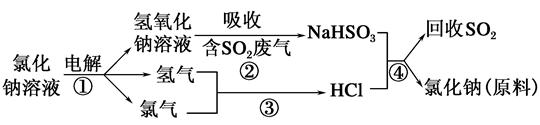
汞(熔点-39℃,沸点356℃)是制造电池、电极等的重要原料,历史上曾用“灼烧辰砂法”制取汞。目前工业上制粗汞的一种流程图如下。
下列分析错误的是
A.“灼烧辰砂法”过程中电子转移的方向和数目可表示为: |
| B.辰砂与氧化钙加热反应时,CaSO4为氧化产物 |
| C.洗涤粗汞可用5%的盐酸代替5%的硝酸 |
| D.减压蒸馏的目的是降低汞的沸点,提高分离效率 |
C
解析试题分析:A、根据化合价的变化,S元素由-2价升高至+4价,失6e?,Hg元素由+2价降低为0价,得2e?,O元素有0价降低为-2价,所以O2得4e?,正确;B、根据流程图,HgS与CaO加热生成Hg和CaSO4、CaS,S元素化合价升高,所以CaSO4为氧化产物,正确;C、盐酸不能与铜反应,所以不能用5%的盐酸代替5%的硝酸,错误;D、减小压强会使物质的沸点降低,所以减压蒸馏的目的是降低汞的沸点,提高分离效率,正确。
考点:本题考查化学工艺流程的分析、氧化还原反应原理。

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
以下金属冶炼方法错误的是:
A.3MnO2 + 4Al 3Mn + 2Al2O3 3Mn + 2Al2O3 | B.2AlCl3(熔融) 2Al + 3Cl2 2Al + 3Cl2 |
C.Fe2O3 + 3CO 2Fe + 3CO2 2Fe + 3CO2 | D.2HgO 2Hg+ O2↑ 2Hg+ O2↑ |
在冶金工业上,均不能用化学还原剂制得的一组金属是
| A.Na Mg Al | B.Na K Zn Fe |
| C.Zn Fe Cu Ag | D.Mg Al Zn Fe |
大气中CO2含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(T1,T2)海水中CO32-浓度与模拟空气中CO2浓度的关系曲线。下列说法不正确的是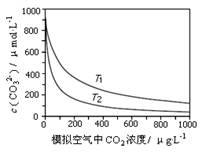
| A.T1>T2 |
| B.海水温度一定时,大气中CO2浓度增加,海水中溶解的CO2随之增大,导致CO32-浓度降低 |
| C.当大气中CO2浓度确定时,海水温度越高,CO32- 浓度越低 |
| D.大气中CO2含量增加时,海水中的珊瑚礁将逐渐溶解 |
下列常见金属的冶炼原理中不合理的是
| | 金属 | 冶炼原理 |
| A | Fe | Fe2O3+3CO 2Fe+3CO2 2Fe+3CO2 |
| B | Hg | 2HgO 2Hg+O2↑ 2Hg+O2↑ |
| C | Mg | 2MgO(熔融)  2Mg+O2↑ 2Mg+O2↑ |
| D | Na | 2NaCl(熔融)  2Na+Cl2↑ 2Na+Cl2↑ |
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如下图所示)
下列有关说法正确的是( )
| A.大量的氰、磷废水排入海洋,易引发赤潮 |
| B.工段②中结晶出的MgCl2·6H2O可在空气中受热分解制无水MgCl2 |
| C.在工段③④⑤中溴元素均被氧化 |
| D.工段①中除去粗盐中的SO、Ca2+、Mg2+、Fe3+等杂质,加入药品的顺序为: |
在冶金工业中,均不能用通常化学还原剂制得的金属组是( )
| A.Na、Mg、Al | B.Na、K、Zn、Fe |
| C.Zn、Fe、Cu、Ag | D.Mg、Al、Zn、Fe |
NaCl是海水中含量最多的盐,除食用外,它还是海洋化学工业原料,下列以NaCl为原料的产品(或物质)是( )
①烧碱 ②纯碱 ③金属钠 ④氯气 ⑤盐酸
| A.全部 | B.只有①②③④ |
| C.只有①②③⑤ | D.只有①②④⑤ |