题目内容
大气中CO2含量的增多除了导致地球表面温度升高外,还会影响海洋生态环境。某研究小组在实验室测得不同温度下(T1,T2)海水中CO32-浓度与模拟空气中CO2浓度的关系曲线。下列说法不正确的是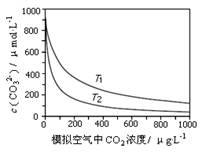
| A.T1>T2 |
| B.海水温度一定时,大气中CO2浓度增加,海水中溶解的CO2随之增大,导致CO32-浓度降低 |
| C.当大气中CO2浓度确定时,海水温度越高,CO32- 浓度越低 |
| D.大气中CO2含量增加时,海水中的珊瑚礁将逐渐溶解 |
C
解析试题分析:A、当大气中CO2浓度确定时,海水温度越高,HCO3--会发生分解,CO32- 浓度越高,所以T1>T2,正确;B、海水温度一定时,大气中CO2浓度增加,海水中溶解的CO2随之增大,导致CO32-转化为HCO32-,浓度降低,正确;C、当大气中CO2浓度确定时,海水温度越高,HCO3-会发生分解,CO32- 浓度越高,错误;大气中CO2含量增加时,海水中溶解的CO2随之增大,导致CO32-浓度降低,从而珊瑚礁会电离子出碳酸根离子补充,珊瑚礁将逐渐溶解,正确。
考点:碳酸盐的转化。

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
汞(熔点-39℃,沸点356℃)是制造电池、电极等的重要原料,历史上曾用“灼烧辰砂法”制取汞。目前工业上制粗汞的一种流程图如下。
下列分析错误的是
A.“灼烧辰砂法”过程中电子转移的方向和数目可表示为: |
| B.辰砂与氧化钙加热反应时,CaSO4为氧化产物 |
| C.洗涤粗汞可用5%的盐酸代替5%的硝酸 |
| D.减压蒸馏的目的是降低汞的沸点,提高分离效率 |
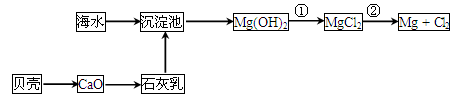
有关海洋中部分资源的利用(如图)的说法不正确的是
| A.工业上利用Cl2与澄清石灰水反应制取漂白粉 |
| B.用MgCl2·6H2O晶体制无水MgCl2,需在HCl气流中加热脱水 |
| C.SO2水溶液吸收Br2的化学方程式为:Br2+SO2+2H2O=H2SO4+2HBr |
| D.粗碘中混有少量HCl和IBr可加入KI进行升华提纯 |
海水是一个巨大的化学资源库,下列有关海水综合利用的说法正确的是( )
| A.海水中含有钾元素,只需经过物理变化不能得到钾单质 |
| B.海水蒸发制海盐的过程中只发生了化学变化 |
| C.从海水中可以得到NaCl,电解熔融NaCl可制备Na |
| D.利用潮汐发电是将化学能转化为电能 |
下列元素①Cl、②Na、③Br、④I、⑤Mg、⑥U属于海水中的微量元素的是
| A.①②⑤ | B.④⑥ | C.①②③④ | D.③④⑤⑥ |
海水中含有氯化镁,是镁的主要来源之一。从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳;②在引有海水的水渠中加入石灰乳、沉降、过滤、洗涤沉淀物;③将沉淀物与盐酸反应,结晶、过滤、干燥产物;④将得到的产物熔融后电解。关于提取镁,下列说法正确的是 ( )。
| A.此法对环境不会造成任何污染 |
| B.沉降、过滤、洗涤沉淀物操作中既有物理变化也有化学变化 |
| C.若提取12 kg Mg,则电子转移1 000 mol |
| D.以上提取镁的过程涉及的离子反应共有3个 |
下列金属的工业制法正确的是( )
| A.制钛:用金属钠置换出氯化钛(TiCl4)溶液中的钛 |
| B.炼铁:用焦炭和空气反应产生的一氧化碳在高温下还原铁矿石中的铁 |
| C.制钠:用海水作原料制得精盐,再电解纯净氯化钠溶液得到金属钠 |
| D.炼铜:用黄铜矿经电解精炼得到纯度为99.9%的铜 |
 发生核裂变,②重氢(2H)发生核聚变,③LiH做野外生氢剂,④海水晒盐
发生核裂变,②重氢(2H)发生核聚变,③LiH做野外生氢剂,④海水晒盐