题目内容
【题目】对水的电离平衡一定不产生影响的微粒是
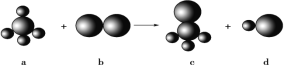
A.![]() B.
B. C.I- D.1s22s22p63s23p6
C.I- D.1s22s22p63s23p6
【答案】C
【解析】
水的电离过程存在电离平衡,电离过程是吸热过程,酸、碱对水的电离起到抑制作用,水解的盐对水的电离起到促进作用。
A.F-核外有10个电子,离子结构示意图是![]() ,由于HF是一元弱酸,所以F-会发生水解反应,消耗水电离产生的H+,使水的电离平衡正向移动,因而会促进水的电离,A不符合题意;
,由于HF是一元弱酸,所以F-会发生水解反应,消耗水电离产生的H+,使水的电离平衡正向移动,因而会促进水的电离,A不符合题意;
B.该符号表示CH3COO-,乙酸根是弱酸阴离子,会发生水解作用,消耗水电离产生的H+,使水的电离平衡正向移动,因而会促进水的电离,B不符合题意;
C.I-是强酸阴离子,不发生水解作用,因此对水的电离无影响,C符合题意;
D.该核外电子排布式可以是阳离子或阴离子的电子排布式,因此不能确定是否影响水的电离,D不符合题意;
故合理选项是C。

练习册系列答案
相关题目
【题目】某温度下,CO(g) + H2O (g)![]() CO2(g)+ H2(g)的平衡常数K=1。该温度下在体积均为1 L的甲、乙两个恒容密闭容器中,投入CO(g) 和 H2O (g)的起始浓度及5min时的浓度如下表所示。
CO2(g)+ H2(g)的平衡常数K=1。该温度下在体积均为1 L的甲、乙两个恒容密闭容器中,投入CO(g) 和 H2O (g)的起始浓度及5min时的浓度如下表所示。
甲 | 乙 | |||
起始浓度 | 5min时浓度 | 起始浓度 | 5min时浓度 | |
c(CO)/mol/L | 0.1 | 0.08 | 0.2 | x |
c(H2O)/mol/L | 0.1 | 0.08 | 0.2 | y |
下列判断不正确的是
A.x = y = 0.16
B.反应开始时,乙中反应速率比甲快
C.甲中0~5min的平均反应速率: v(CO)=0.004"mol/(L·min)
D.平衡时,乙中H2O的转化率是50%,c(CO)是甲中的2倍