题目内容
关于锂的结构和性质的判断:①与水反应比钠剧烈;②锂的原子半径比钠小;③锂的氧化物暴露于空气中易吸收CO2;④锂的阳离子的最外层电子数和钠离子的最外层电子数相同;⑤锂是还原剂.其中错误的是( )
| A、只有①和⑤ |
| B、只有②和③ |
| C、只有③和⑤ |
| D、只有①和④ |
考点:碱金属的性质,原子结构与元素的性质
专题:元素周期律与元素周期表专题
分析:根据元素周期律中碱金属族的变化规律分析判断,碱金属元素中随着原子序数的递增,金属性逐渐增强,失电子能力逐渐增强,原子半径逐渐增大,据此分析解答.
解答:
解:①碱金属元素中随着原子序数的递增,金属性逐渐增强,失电子能力逐渐增强,所以与水反应不如钠剧烈,故错误;
②碱金属元素中随着原子序数的递增,原子半径逐渐增大,所以锂原子半径小于钠,故正确;
③氧化锂是碱性氧化物,所以它的氧化物在空气中易吸收二氧化碳,故正确;
④锂原子失去最外层电子后次外层变成最外层,锂离子最外层有2个电子,钠离子最外层有8个电子,所以它的阳离子最外层电子数与钠的阳离子不同,故错误;
⑤锂原子最外层有1个电子,容易失去电子,所以它是还原剂,故正确.
故选D.
②碱金属元素中随着原子序数的递增,原子半径逐渐增大,所以锂原子半径小于钠,故正确;
③氧化锂是碱性氧化物,所以它的氧化物在空气中易吸收二氧化碳,故正确;
④锂原子失去最外层电子后次外层变成最外层,锂离子最外层有2个电子,钠离子最外层有8个电子,所以它的阳离子最外层电子数与钠的阳离子不同,故错误;
⑤锂原子最外层有1个电子,容易失去电子,所以它是还原剂,故正确.
故选D.
点评:本题涉及元素周期律知识的考查,同主族元素的性质具有相似性和递变性,注意知识的迁移应用,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1000C时,将0.40mol二氧化氮气体充入2L密闭容器中,发生反应2NO2(g)?N2O4(g)△H=-57kJ?mol-1,每隔一段时间对该容器内的物质进行分析.得到数据如下表所示:
下列说法正确的是( )
| 时间/s | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
| A、反应开始20s内,用二氧化氮表示的平均反应速率为0.005mol?L-1?s-1 |
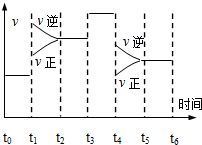
| B、保持其他条件不变,若起始时向容器中充入0.30mol NO2和0.10mol N2O4,则此时v正<v逆 |
| C、80s时向容器中再加入0.32mol氮气,同时将容器扩大为4L,则平衡不移动 |
| D、保持其他条件不变,向容器中再充入是0.20mol NO2,达到平衡时,NO2的体积分数减小 |
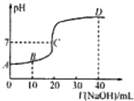 25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL 0.1000mol/L的CH3COOH.滴定曲线如图所示.下列分析错误的是( )
25℃时,用浓度为0.1000mol/L的NaOH溶液滴定20.00mL 0.1000mol/L的CH3COOH.滴定曲线如图所示.下列分析错误的是( )| A、C点的溶液:c(CH3COO-)+c(CH3COOH)>c(Na-) |
| B、B点的溶液:c(CH3COO-)>(Na+)>c(H-)>c(OH-) |
| C、A点的纵坐标值为1 |
| D、D点溶液2c(CH3COOH)+c(H+)=c(OH-)-c(CH3COO-) |
a、b、c、d都是短周期元素,原子半径d>c>a>b,其中a、b处在同一周期,a、c处在同一主族.c原子核内质子数等于a、b原子核内质子数之和,c原子最外层上的电子数是d原子最外层电子数的4倍.下列说法中不正确的( )
| A、a、c两元素位于元素周期表的IVA族 |
| B、d单质在b单质中燃烧生成的化合物中阴阳离子个数比为1:1 |
| C、单质c可以和d的最高价氧化物的水化物发生反应 |
| D、工业上可用单质a冶炼单质c |
V L含有(NH4)2SO4、NH4NO3的混合溶液,加入a mol NaOH后加热,恰好使NH3全部逸出;又加入b mol BaCl2,刚好使SO42-完全沉淀.则原混合溶液中NH4NO3的物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
在给定条件下可能大量共存的离子组是( )
| A、在含有大量AlO2-的溶液中:Cu2+、Na+、Br-、HCO3- |
| B、使石蕊变红的溶液中:K+、I-、MnO4-、SO42- |
| C、水电离的H+浓度c(H+)=10-12mol?L-1的溶液中:NH4+、Na+、Cl-、NO3- |
| D、加入Mg能放出H2的溶液中:Mg2+、Ba2+、ClO-、Br- |
下列说法正确的是( )
| A、石油分馏和煤的干馏都是物理变化 |
| B、塑料和蚕丝都是天然高分子化合物 |
| C、淀粉和纤维素水解的最终产物都是葡萄糖 |
| D、易溶于汽油、酒精、苯的物质一定是有机物 |
 2013年冬季,雾霾天气多次肆虐我国东部地区.其中汽车尾气是造成空气污染的原因之一,研究控制汽车尾气成为保护环境的首要任务.
2013年冬季,雾霾天气多次肆虐我国东部地区.其中汽车尾气是造成空气污染的原因之一,研究控制汽车尾气成为保护环境的首要任务.