题目内容
4.“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题.(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式,并在方框内填上系数.
□C+□KMnO4+□H2SO4=□CO2↑+□MnSO4+□K2SO4+□H2O
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如下二组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
②实验2条件下平衡常数表达式K=$\frac{c({CO}_{2})c({H}_{2})}{c(CO)c({H}_{2}O)}$,该反应为放热(填“吸热”或“放热”)反应.
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H1=-1275.6kJ/mol
②2CO (g)+O2(g)=2CO2(g)△H2=-566.0kJ/mol
③H2O(g)=H2O(l)△H3=-44.0kJ/mol
写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-354.8kJ/mol.
分析 (1)反应中C元素的化合价升高,锰元素的化合价升高,可结合氧化还原反应中得失电子数相等先确定氧化剂KMnO4及其还原产物的系数、还原剂C及其氧化产物CO2的系数,再结合原子守恒推断其它反应物和生成物的系数并确定未知物的组成与系数;
(2)①由表中数据可知,CO的物质的量变化量为4mol-2.4mol=1.6mol,根据v=$\frac{\frac{△n}{V}}{△t}$ 计算v(CO),再利用速率之比等于化学计量数之比计算v(CO2);
②利用三段式计算平衡时,各组分的物质的量,该反应是气体体积不变的反应,故利用物质的量代替浓度代入平衡常数表达式计算平衡常数;第二组温度比第一组高,反应物物质的量比第一组减半,但是平衡时CO2的物质的量比第一组的一半少,表明该反应为放热反应;
(3)根据甲醇不完全燃烧生成一氧化碳和气态水,结合①②热化学方程式运用盖斯定律计算出反应热并写出热化学方程式.
解答 解:(1)高锰酸钾中锰元素化合价降低7-2=5价,碳元素化合价升高4-0=4价,化合价升高数=化合价降低数,所以高锰酸钾前的系数是4,碳单质前的系数是5,根据原子守恒,二氧化碳前是5,硫酸锰前是4,硫酸钾前面是2,根据硫酸跟守恒,所以硫酸前面是6,据氧原子和氢原子守恒,产物少6个水分子,得化学反应方程式为5C+4KMnO4+6 H2SO4=5CO2↑+4MnSO4+2K2SO4+6H2O,故答案为:5;4;6;5;4;2;6H2O;
(2)①由表中数据可知,CO的物质的量变化量为4mol-2.4mol=1.6mol,v(CO)=$\frac{\frac{△n}{△V}}{△t}=\frac{\frac{1.6mol}{2L}}{6mil}=\frac{2}{15}$mol/(L•min),速率之比等于化学计量数之比,故v(CO2)=v(CO)=$\frac{2}{15}$mol/(L•min)=0.13mol/(L•min),故答案为:0.13mol/(L•min);
②平衡时CO的物质的量为1.6mol,则:
CO(g)+H2O(g)?CO2(g)+H2(g),
开始(mol):2 1 0 0
变化(mol):0.4 0.4 0.4 0.4
平衡(mol):1.6 0.6 0.4 0.4
该反应前后气体体积不变,故利用物质的量代替浓度计算平衡常数,故900℃时该反应平衡常数k=$\frac{c(C{O}_{2})c({H}_{2})}{c(CO)c({H}_{2}O)}=\frac{0.4×0.4}{1.6×0.6}$=0.17,实验1中CO的转化率为$\frac{1.6}{4}$×100%=40%,实验2中CO的转化率为$\frac{0.4}{2}$×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动,正反应放热,
故答案为:$\frac{c({CO}_{2})c({H}_{2})}{c(CO)c({H}_{2}O)}$;放热;
(3)已知:①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1275.6kJ/mol
②2CO (g)+O2(g)=2CO2 (g)△H2=-566.0kJ/mol
根据盖斯定律,①-②得2CH3OH(l)+2O2(g)=2CO(g)+4H2O(g),该反应的反应热△H=-1275.6kJ/mol-(-566.0kJ/mol)=-709.6kJ/mol
故该反应热化学方程式为:CH3OH(l)+O2(g)=CO(g)+2 H2O(g)△H=-354.8kJ/mol,
故答案为:CH3OH(l)+O2(g)=CO(g)+2H2O(g)△H=-354.8kJ/mol.
点评 本题考查较为综合,涉及化学平衡常数、化学平衡计算、热化学方程式书写、氧化还原方程式配平等,题目难度中等.

| A. | 118号元素应该位于周期表的0族元素氡之下 | |
| B. | 制造出的118号元素的一个原子中子数为179,则该原子的摩尔质量297 | |
| C. | 目前还没有发现117号元素,推测117号元素应该属于金属元素 | |
| D. | 118号原子可衰变成116号元素,该过程不属于化学变化 |
| A. | 1 mol Cu2S参加反应时有10 mol电子转移 | |
| B. | 参加反应的n(Cu2S):n(HNO3)=1:5 | |
| C. | 反应中Cu2S作还原剂 | |
| D. | 产物n[Cu(NO3)2]:n[CuSO4]=l:1 |
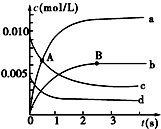 在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:
在2L密闭容器中,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如下表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)图中表示O2变化的曲线是d.用NO2表示从0~2s内该反应的平均速率v=3×10-3mol/(L•s).
(3)能说明该反应已经达到平衡状态的是ad.
a.NO、O2、NO2的浓度不变
b.v(NO)=2v(O2)c.NO、O2、NO2的分子数之比为2:1:2
d.v逆(NO2)=2v正(O2)
(4)能使该反应的反应速率增大的是acd.
a.适当升高温度 b.及时分离出NO2气体
c.增大O2的浓度 d.选择高效的催化剂.
| A. | 一个小黑点表示一个电子 | B. | 黑点的多少表示电子个数的多少 | ||
| C. | 表示电子运动的轨迹 | D. | 电子在核外空间出现机会的多少 |
| A. | Na2O2 | B. | HCl | C. | KOH | D. | CaCl2 |
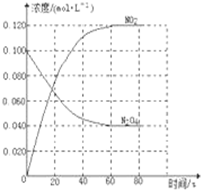 在容积为1.00L的容器中,通入一定量的N2O4,发生反应,随温度升高,混合气体的颜色变深.回答下列问题:
在容积为1.00L的容器中,通入一定量的N2O4,发生反应,随温度升高,混合气体的颜色变深.回答下列问题: