题目内容
【题目】莫尔盐[硫酸亚铁铵,(NH4)2Fe(SO4)26H2O,Mr=392]是一种重要的还原剂,在空气中比一般的亚铁盐稳定,易溶于水,难溶于乙醇。某学习小组设计如下实验制备少量的莫尔盐并测定其纯度。

回答下列问题:
Ⅰ.制取莫尔盐
i.连接装置,检査装置气密性。将13.2g(NH4)2SO4晶体置于三颈烧瓶B中,将6.0g洁净铁屑加入锥形瓶中。
ii.打开仪器a瓶塞,关闭活塞K3,打开K2、K1,加完55.0mL2mol·L-1稀硫酸后关闭K1。
iii.待大部分铁粉溶解后,打开K3、关闭K2,A中浅绿色溶液流入B。
iv.关闭活塞K2、K3,采用100℃水浴蒸发三颈烧瓶中水分,液面产生晶膜时,停止加热,冷却结晶、过滤、洗涤晶体。
(1)仪器a的名称是___。
(2)操作iii中浅绿色溶液会流入B的原因是___。
(3)操作iv中洗涤晶体所用试剂是___(填标号)。
A.水 B.无水乙醇 C.硫酸溶液
Ⅱ.为测定所得莫尔盐晶体纯度,取mg该样品配制成1L溶液,分别设计如下两个实验方案,请回答:
方案一:取20.00mL所配硫酸亚铁铵溶液用0.1000mol·L-1的酸性K2Cr2O7溶液进行滴定。重复三次。(已知:Cr2O72-还原产物为Cr3+)
(4)写出此反应的离子方程式___。
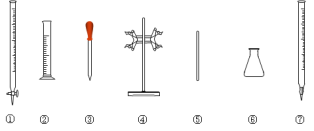
(5)滴定时必须选用的仪器是___。(填标号)
方案二:取20.00mL所配硫酸亚铁铵溶液进行如下实验。
![]()
(6)莫尔盐晶体纯度为___。(用含m、w的式子表示)
(7)若实验操作都正确,但方案一的测定结果总是小于方案二,其可能原因为__。
【答案】分液漏斗 A中产生H2使其压强大于B B 6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O ①④⑥ ![]() ×100% 部分Fe2+被空气氧化
×100% 部分Fe2+被空气氧化
【解析】
(1)仪器a的名称是分液漏斗;
(2)A中产生H2使其压强大于B;
(3)摩尔盐易溶于水而难溶于乙醇,洗涤摩尔盐时摩尔盐不能溶解于洗涤剂;
(4)Cr2O72-还原产物为 Cr3+,则K2Cr2O7 具有氧化性,摩尔盐中亚铁离子被氧化生成铁离子,同时还生成水,根据反应物和生成物书写离子方程式;
(5)酸性 K2Cr2O7 溶液具有强氧化性和酸性,应该盛放在酸式滴定管中,所以该实验滴定时需要的仪器有酸式滴定管、滴定管夹、锥形瓶;
(6)得到的沉淀是BaSO4,n(BaSO4)=![]() mol,根据硫酸根离子守恒得(NH4)2Fe(SO4)26H2O~2BaSO4,则n[(NH4)2Fe(SO4)2
mol,根据硫酸根离子守恒得(NH4)2Fe(SO4)26H2O~2BaSO4,则n[(NH4)2Fe(SO4)2![]() 6H2O]=
6H2O]=![]() n(BaSO4)=
n(BaSO4)=![]() mol,m[(NH4)2Fe(SO4)2
mol,m[(NH4)2Fe(SO4)2![]() 6H2O]=
6H2O]=![]() mol×392g/mol×
mol×392g/mol×![]() =
=![]() g,摩尔盐纯度=
g,摩尔盐纯度=![]() ×100%;
×100%;
(7)Fe2+不稳定,易被空气氧化。
(1)仪器a的名称是分液漏斗;
(2)A中产生H2使其压强大于B,液体从压强大的装置流入压强小的装置,所以浅绿色溶液会流入 B;
(3)摩尔盐易溶于水而难溶于乙醇,洗涤摩尔盐时摩尔盐不能溶解于洗涤剂,所以应该选取乙醇洗涤摩尔盐,答案为B;
(4)Cr2O72-还原产物为 Cr3+,则K2Cr2O7 具有氧化性,摩尔盐中亚铁离子被氧化生成铁离子,同时还生成水,根据反应物和生成物书写离子方程式为6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O;
(5)酸性 K2Cr2O7 溶液具有强氧化性和酸性,应该盛放在酸式滴定管中,所以该实验滴定时需要的仪器有酸式滴定管、滴定管夹、锥形瓶,所以应该选取①④⑥;
(6)得到的沉淀是BaSO4,n(BaSO4)=![]() mol,根据硫酸根离子守恒得(NH4)2Fe(SO4)26H2O~2BaSO4,则n[(NH4)2Fe(SO4)26H2O]=
mol,根据硫酸根离子守恒得(NH4)2Fe(SO4)26H2O~2BaSO4,则n[(NH4)2Fe(SO4)26H2O]=![]() n(BaSO4)=
n(BaSO4)=![]() mol,m[(NH4)2Fe(SO4)26H2O]=
mol,m[(NH4)2Fe(SO4)26H2O]=![]() mol×392g/mol×
mol×392g/mol×![]() =
=![]() g,摩尔盐纯度=
g,摩尔盐纯度=![]() ×100%=
×100%=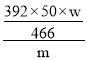 ×100%=
×100%=![]() ×100%;
×100%;
(7)Fe2+不稳定,易被空气氧化,导致方法一测定值偏小。

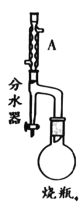
【题目】实验室制备甲基丙烯酸甲酯的反应装置示意图和有关信息如下:
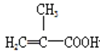 +CH3OH
+CH3OH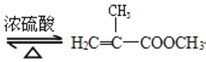 +H2O
+H2O
药品 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度(gcm-3) |
甲醇 | 32 | -98 | -64.5 | 与水混溶,易溶于有机溶剂 | 0.79 |
甲基丙烯酸 | 86 | 15 | 161 | 溶于热水,易溶于有机剂 | 1.01 |
甲基丙烯酸甲酯 | 100 | -48 | 100 | 微溶于水,易溶于有机溶剂 | 0.944 |
已知甲基丙烯酸甲酯受热易聚合;甲基丙烯酸甲酯在盐溶液中溶解度较小;CaCl2可与醇结合形成复合物;
实验步骤:
①向100mL烧瓶中依次加入:15mL甲基丙烯酸、2粒沸石、10mL无水甲醇、适量的浓硫酸;
②在分水器中预先加入水,使水面略低于分水器的支管口,通入冷凝水,缓慢加热 烧瓶。在反应过程中,通过分水器下部的旋塞分出生成的水,保持分水器中水层液面的高度不变,使油层尽量回到圆底烧瓶中;
③当 ,停止加热;
④冷却后用试剂 X 洗涤烧瓶中的混合溶液并分离;
⑤取有机层混合液蒸馏,得到较纯净的甲基丙烯酸甲酯。请回答下列问题:
(1)A装置的名称是_____。
(2)请将步骤③填完整____。
(3)上述实验可能生成的副产物结构简式为_____(填两种)。
(4)下列说法正确的是______
A.在该实验中,浓硫酸是催化剂和脱水剂
B.酯化反应中若生成的酯的密度比水大,不能用分水器提高反应物的转化率
C.洗涤剂X是一组试剂,产物要依次用饱和Na2CO3、饱和CaCl2溶液洗涤
D.为了提高蒸馏速度,最后一步蒸馏可采用减压蒸馏;该步骤一定不能用常压蒸馏
(5)实验结束收集分水器分离出的水,并测得质量为2.70g,计算甲基丙烯酸甲酯的产率约为_____。实验中甲基丙烯酸甲酯的实际产率总是小于此计算值,其原因不可能是_____。
A.分水器收集的水里含甲基丙烯酸甲酯
B.实验条件下发生副反应
C.产品精制时收集部分低沸点物质
D.产品在洗涤、蒸发过程中有损失