题目内容
【题目】“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视。所以“低碳经济”正成为科学家研究的主要课题。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
___ C+ ___ KMnO4+ H2SO4 = ____CO2↑+ ____MnSO4 + ____K2SO4+
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)![]() CO2(g)+H2(g),得到如下二组数据:
CO2(g)+H2(g),得到如下二组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
①实验1中以CO2表示的化学反应速率为__________(保留小数点后二位数,下同)。
②实验2条件下平衡常数K=_________,该反应为 _____(填“吸”或“放”)热反应。
(3)已知在常温常压下:
① 2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g) ΔH = -1275.6 kJ/mol
② 2CO (g)+ O2(g) = 2CO2(g) ΔH = -566.0 kJ/mol
③ H2O(g) = H2O(l) ΔH = -44.0 kJ/mol
写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式:_____________。
(4)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。

①该电池负极的电极反应为:_______________。
②该电池工作时,溶液中的OH-向______极移动。
【答案】 5 C + 4KMnO4 + 6 H2SO4 = 5CO2↑+ 4MnSO4 + 2K2SO4+ 6H2O 0.13mol/(L·min) 0.17 放 CH3OH(l)+O2(g)=CO(g)+2H2O(g)ΔH=-354.8KJ/mol CH3OH+8OH— —6e-=CO32-+6 H2O 负
【解析】(1)由反应方程式可知,C元素从0价升高为+4价,Mn元素从+7价降低为+2价,所以最小公倍数为20,则配平后的方程式为 5 C + 4KMnO4 + 6 H2SO4 = 5CO2↑+ 4MnSO4 + 2K2SO4+ 6H2O;
(2)①由表中实验1的数据,结合反应方程式可知,n(CO2)起始=0,平衡时n(CO2)平衡=n(H2)平衡=1.6mol,则以CO2表示的化学反应速率为=![]() = 1.3(L·min);②实验2中各物质的平衡浓度为c(CO2)平衡=c(H2)平衡=0.2mol/L,c(CO)平衡=0.8mol/L,c(H2O)平衡=0.3mol/L,则K2=
= 1.3(L·min);②实验2中各物质的平衡浓度为c(CO2)平衡=c(H2)平衡=0.2mol/L,c(CO)平衡=0.8mol/L,c(H2O)平衡=0.3mol/L,则K2= ![]() =
=![]() = 0.17;同理求出实验1的K1 = 2.7,可见,当温度升高时,平衡常数K值减小,即平衡向左移动,则该反应为放热反应;
= 0.17;同理求出实验1的K1 = 2.7,可见,当温度升高时,平衡常数K值减小,即平衡向左移动,则该反应为放热反应;
(3)根据要求甲醇不完全燃烧生成一氧化碳和水的化学方程式为CH3OH+O2=CO +2H2O,根据盖斯定律(①—②)/2 可得CH3OH(l)+O2(g)=CO(g) +2H2O(g) ΔH=-354.8KJ/mol;
(4)该装置的原理实质就是甲醇在碱性条件下的燃烧,反应的离子方程式为2CH3OH+3O2+4OH-![]() 2CO32-+6H2O,所以通氧气的一极为正极,其电极反应式为O2+2H2O+4e-=4OH-,则甲醇在负极反应,其电极反应式为CH3OH+8OH— —6e-=CO32-+6 H2O;根据原电池工作原理,在电解质溶液中,阴离子向负极移动,所以溶液中的OH-向负极即甲醇的一极移动。
2CO32-+6H2O,所以通氧气的一极为正极,其电极反应式为O2+2H2O+4e-=4OH-,则甲醇在负极反应,其电极反应式为CH3OH+8OH— —6e-=CO32-+6 H2O;根据原电池工作原理,在电解质溶液中,阴离子向负极移动,所以溶液中的OH-向负极即甲醇的一极移动。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案【题目】生活中为了延长鲜花的寿命,通常会在花瓶中加入鲜花保鲜剂。下表是0.5 L某种鲜花保鲜剂中含有的成分及含量,阅读后回答下列问题:
成分 | 质量(g) | 摩尔质量(g/mol) |
蔗糖(C12H22O11) | 25.00 | 342 |
硫酸钾(K2SO4) | 0.25 | 174 |
高锰酸钾(KMnO4) | 0.25 | 158 |
阿司匹林(C9H8O4) | 0.17 | 180 |
硝酸银(AgNO3) | 0.02 | 170 |
(1)鲜花保鲜剂的下列成分中,属于电解质的是________(填字母)。
a.蔗糖 b.硫酸钾
c.高锰酸钾 d.硝酸银
(2)欲配制480 mL该鲜花保鲜剂,现已提供下列仪器:
①胶头滴管、②量筒、③烧杯、④药匙、⑤电子天平,如要完成实验,缺少的玻璃仪器还有________(写仪器名称)。
(3)写出该鲜花保鲜剂中K+的物质的量浓度的计算式:________(不必化简)。
(4)将m g蔗糖完全燃烧后的产物通过足量的Na2O2固体,充分反应后,固体增加的质量________(填“>”“=”或“<”)m g。
【题目】某学习小组研究溶液中Fe2+的稳定性,进行如下实验,记录结果。
【实验Ⅰ】
物质 | 0 min | 1min | 1h | 5h |
FeSO4 | 淡黄色 | 桔红色 | 红色 | 深红色 |
((NH4)2Fe(SO4)2 | 几乎无色 | 淡黄色 | 黄色 | 桔红色 |
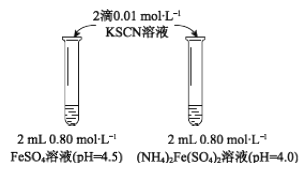
(1)上述(NH4)2Fe(SO4)2溶液pH小于FeSO4的原因是_____________(用离子方程式表示)。溶液的稳定性:FeSO4_______(NH4)2Fe(SO4)2(填“>”或“<”)。
(2)甲同学提出实验Ⅰ中两溶液的稳定性差异可能是(NH4)2Fe(SO4)2溶液中的NH4+保护了Fe2+,因为NH4+具有还原性。进行【实验Ⅱ】,否定了该观点,请补全该实验。
操作 | 现象 |
取__________,滴加_______,观察。 | 与实验Ⅰ中(NH4)2Fe(SO4)2溶液现象相同。 |
(3)乙同学提出【实验Ⅰ】中两溶液的稳定性差异是溶液酸性不同导致,进行【实验III】,分别配制0.8 mol![]() L—pH为1、2、3、4的FeSO4溶液,观察,发现pH=1的FeSO4溶液长时间无明显变化,pH越大,FeSO4溶液变黄的时间越短。
L—pH为1、2、3、4的FeSO4溶液,观察,发现pH=1的FeSO4溶液长时间无明显变化,pH越大,FeSO4溶液变黄的时间越短。
资料显示:亚铁盐溶液中存在反应4Fe2++O2+10H2O ![]() 4Fe(OH)3+8H+
4Fe(OH)3+8H+
由【实验III】,乙同学可得出实验的结论是___________________________,原因是___________________________________________________________。
(4)进一步研究在水溶液中
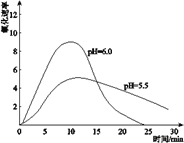
(5)综合以上实验,增强Fe2+稳定性的措施有__________________________。
(6)向溶液中加入一定量H2O2氧化Fe2+。为确定加入H2O2的量,需先用K2Cr2O7标准溶液滴定滤液中的Fe2+,离子方程式如下:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
①在向滴定管注入K2Cr2O7标准溶液前,滴定管需要检漏、用蒸馏水洗涤和_____________________,应选用___________式滴定管。
②若滴定xmL滤液中的Fe2+,消耗amol·L—1K2Cr2O7标准溶液bmL,则滤液中c(Fe2+)=______mol·L-1。