题目内容
由甲、乙两人组成的实验小组,在同样的实验条件下,用同样的实验仪器和方法步骤进行两组中和热测定的实验,实验试剂及其用量如表所示.
(1)实验过程中需要用到的玻璃仪器有烧杯、温度计、 、 .
(2)实验测得的温度是①的起始温度13.0℃、终了温度19.8℃;②的起始温度13.0℃、终了温度19.3℃.则△H1和△H2的大小关系是 ,导致这种差异的主要原因是 .
| 反应物 | 起始温度(t1)/℃ | 终了温度(t2)/℃ | 中和热(kJ?mol-1) |
| ①1.0 mol/L HCl溶液50 mL、 1.1 mol/L NaOH溶液50 mL |
13.0℃[ | △H1[ | |
| ②1.0 mol/L HCl溶液50 mL、 1.1 mol/LNH3?H2O溶液50 mL |
13.0℃ | △H2 |
(2)实验测得的温度是①的起始温度13.0℃、终了温度19.8℃;②的起始温度13.0℃、终了温度19.3℃.则△H1和△H2的大小关系是
考点:中和热的测定
专题:化学反应中的能量变化
分析:(1)根据量热计的构造和实验步骤来确定实验的仪器;
(2)弱电解质存在电离平衡,电离过程是吸热过程.
(2)弱电解质存在电离平衡,电离过程是吸热过程.
解答:
解:(1)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、搅拌器以及量筒;
故答案为:环形玻璃搅拌棒;量筒;
(2)NH3?H2O是弱电解质,存在电离平衡,电离过程是吸热程,稀氨水和1.0 mol/L HCl溶液恰好完全反应放热偏小,终了温度偏低,反应热数值偏小,但反应热是负值,所以△H1<△H2,
故答案为:△H1<△H2;NH3?H2O是弱电解质,存在电离平衡,电离过程是吸热程.
故答案为:环形玻璃搅拌棒;量筒;
(2)NH3?H2O是弱电解质,存在电离平衡,电离过程是吸热程,稀氨水和1.0 mol/L HCl溶液恰好完全反应放热偏小,终了温度偏低,反应热数值偏小,但反应热是负值,所以△H1<△H2,
故答案为:△H1<△H2;NH3?H2O是弱电解质,存在电离平衡,电离过程是吸热程.
点评:本题考查了中和热的测定方法,题目难度不大,注意掌握测定中和热的正确方法,明确实验操作过程中关键在于尽可能减少热量散失,使测定结果更加准确.

练习册系列答案
相关题目
现有反应:CO(g)+H2O(g)?CO2(g)+H2(g),已知1mol CO和2mol H2O(g)在一定条件下反应达平衡时生成0.7mol CO2,若其它条件不变,把2mol H2O(g)改成4mol,达平衡时生成CO2可能是( )
| A、1.2 mol |
| B、0.83 mol |
| C、1.5 mol |
| D、2 mol |
下列氯化物中,不能通过单质之间直接制取的是( )
| A、FeCl2 |
| B、FeCl3 |
| C、CuCl |
| D、CuCl2 |
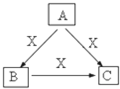 A、B、C、X是中学化学常见物质,均由前18号元素组成,转化关系如图.请针对以下三种不同情况回答:
A、B、C、X是中学化学常见物质,均由前18号元素组成,转化关系如图.请针对以下三种不同情况回答: