题目内容
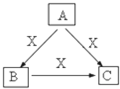 A、B、C、X是中学化学常见物质,均由前18号元素组成,转化关系如图.请针对以下三种不同情况回答:
A、B、C、X是中学化学常见物质,均由前18号元素组成,转化关系如图.请针对以下三种不同情况回答:(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,B是白色胶状沉淀.
①A中含有的金属元素为
②该金属元素的单质与某氧化物在高温下反应,可用于焊接铁轨及定向爆破,反应的化学反应方程式为
(2)若A为固态非金属单质,且有多种同素异形体,B为无色无味有毒的可燃气体,
①B的化学式为
②镁条能在C中剧烈燃烧,反应的化学方程式为:
(3)若A、B、C的焰色反应均呈黄色,它们水溶液均为碱性,C是一种常见的食用碱,也是焙制糕点所用的发酵粉的主要成分之一.
①B生成C的反应方程式是
②自然界中存在B、C和H2O按一定比例结晶而成的固体.取一定量该固体溶于水配成200mL溶液,测得溶液中金属阳离子的浓度为0.5mol/L.若取相同质量的固体加热至恒重,剩余固体的质量为
考点:无机物的推断,常见金属元素的单质及其化合物的综合应用
专题:推断题,几种重要的金属及其化合物
分析:A、B、C、X是中学化学常见物质,均由前18号元素组成,
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,B是白色胶状沉淀,由转化关系可知,A含有铝离子,B为氢氧化铝,C含有偏铝酸根,X为氢氧化钠;
(2)若A为固态非金属单质,且有多种同素异形体,B为无色无味有毒的可燃气体,结合转化关系可知,A为碳、B为CO、C为二氧化碳、X为氧气;
(3)若A、B、C的焰色反应均呈黄色,含有钠元素,水溶液均为碱性,C是一种常见的食用碱,也是焙制糕点所用的发酵粉的主要成分之一,结合转化关系可知,A为氢氧化钠,B为碳酸钠,C为碳酸氢钠,X为二氧化碳.
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,B是白色胶状沉淀,由转化关系可知,A含有铝离子,B为氢氧化铝,C含有偏铝酸根,X为氢氧化钠;
(2)若A为固态非金属单质,且有多种同素异形体,B为无色无味有毒的可燃气体,结合转化关系可知,A为碳、B为CO、C为二氧化碳、X为氧气;
(3)若A、B、C的焰色反应均呈黄色,含有钠元素,水溶液均为碱性,C是一种常见的食用碱,也是焙制糕点所用的发酵粉的主要成分之一,结合转化关系可知,A为氢氧化钠,B为碳酸钠,C为碳酸氢钠,X为二氧化碳.
解答:
解:A、B、C、X是中学化学常见物质,均由前18号元素组成,
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,B是白色胶状沉淀,由转化关系可知,A含有铝离子,B为氢氧化铝,C含有偏铝酸根,X为氢氧化钠,
①A中含有的金属元素为Al,故答案为:Al;
②Al与氧化铁发生铝热反应可用于焊接铁轨及定向爆破,此反应的化学方程式为:2Al+Fe2O3
Al2O3+2Fe,故答案为:2Al+Fe2O3
Al2O3+2Fe;
(2)若A为固态非金属单质,且有多种同素异形体,B为无色无味有毒的可燃气体,结合转化关系可知,A为碳、B为CO、C为二氧化碳、X为氧气;
①B的化学式为CO,故答案为:CO;
②镁条能在CO2中剧烈燃烧生成碳与氧化镁,反应的化学方程式为:2Mg+CO2
2MgO+C,故答案为:2Mg+CO2
2MgO+C;
(3)若A、B、C的焰色反应均呈黄色,含有钠元素,水溶液均为碱性,C是一种常见的食用碱,也是焙制糕点所用的发酵粉的主要成分之一,结合转化关系可知,A为氢氧化钠,B为碳酸钠,C为碳酸氢钠,X为二氧化碳,
①B生成C的反应方程式是:Na2CO3+CO2+H2O=2NaHCO3,故答案为:Na2CO3+CO2+H2O=2NaHCO3;
②自然界中存在B、C和H2O按一定比例结晶而成的固体,取一定量该固体溶于水配成200mL溶液,测得溶溶中金属阳离子的浓度为0.5mol/L,即钠离子浓度为0.5mol/L,取相同质量的固体加热至恒重,剩余固体为碳酸钠,根据钠离子守恒可知,碳酸钠的质量为
×0.2L×0.5mol/L×106g/mol=5.3g,
故答案为:5.3 g.
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在,B是白色胶状沉淀,由转化关系可知,A含有铝离子,B为氢氧化铝,C含有偏铝酸根,X为氢氧化钠,
①A中含有的金属元素为Al,故答案为:Al;
②Al与氧化铁发生铝热反应可用于焊接铁轨及定向爆破,此反应的化学方程式为:2Al+Fe2O3
| ||
| ||
(2)若A为固态非金属单质,且有多种同素异形体,B为无色无味有毒的可燃气体,结合转化关系可知,A为碳、B为CO、C为二氧化碳、X为氧气;
①B的化学式为CO,故答案为:CO;
②镁条能在CO2中剧烈燃烧生成碳与氧化镁,反应的化学方程式为:2Mg+CO2
| ||
| ||
(3)若A、B、C的焰色反应均呈黄色,含有钠元素,水溶液均为碱性,C是一种常见的食用碱,也是焙制糕点所用的发酵粉的主要成分之一,结合转化关系可知,A为氢氧化钠,B为碳酸钠,C为碳酸氢钠,X为二氧化碳,
①B生成C的反应方程式是:Na2CO3+CO2+H2O=2NaHCO3,故答案为:Na2CO3+CO2+H2O=2NaHCO3;
②自然界中存在B、C和H2O按一定比例结晶而成的固体,取一定量该固体溶于水配成200mL溶液,测得溶溶中金属阳离子的浓度为0.5mol/L,即钠离子浓度为0.5mol/L,取相同质量的固体加热至恒重,剩余固体为碳酸钠,根据钠离子守恒可知,碳酸钠的质量为
| 1 |
| 2 |
故答案为:5.3 g.
点评:本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合运用的考查,熟悉元素化合物知识是关键,题目难度中等,(1)中B为白色胶状沉淀及(3)中焰色为突破口,注意(3)中利用原子守恒进行计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
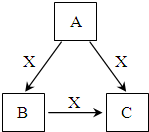 A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示的转化关系(其他产物已略去),下列说法不正确的是( )
A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示的转化关系(其他产物已略去),下列说法不正确的是( )| A、若X为O2,则A可能是金属单质,也可能是非金属单质 |
| B、若X为O2,则A可能是化合物 |
| C、若X为NaOH溶液,则A可能是化合物 |
| D、若X为NaOH溶液,则A可能为单质 |
下列说法正确的是( )
| A、第ⅠA族的金属单质与水反应一定比第ⅡA族的金属单质剧烈 |
| B、第二周期元素的最高正价和最低负价的绝对值之和等于8 |
| C、同周期主族元素的原子形成简单离子的电子层结构相同 |
| D、第ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |

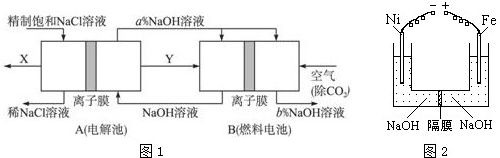
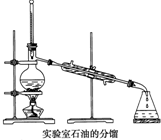 实验室中常采用如图所示装置进行石油分馏,请回答下列问题:
实验室中常采用如图所示装置进行石油分馏,请回答下列问题: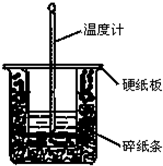 50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: