题目内容
5.下列说法中正确的是(NA为阿伏加德罗常数)( )| A. | 48gO3气体含有NA个O3分子 | |
| B. | 7.8gNa2O2含有0.2NA个阴离子 | |
| C. | 27gAl含有电子的总数为3NA个 | |
| D. | 标准状况下,22.4LH2O中含有NA个氧原子 |
分析 A.质量转化为物质的量,结合N=nNA计算;
B.过氧化钠是由钠离子与过氧离子构成;
C.1个铝原子含有13个电子;
D.气体摩尔体积适用对象为气体.
解答 解:A.48gO3气体的物质的量为$\frac{48g}{48g/mol}$=1mol,含有臭氧分子数为NA,故A正确;
B.7.8g过氧化钠的物质的量为0.1mol,含有阴离子的总是为0.1mol,0.1NA个阴离子,故B错误;
C.27gAl物质的量为1mol,含有电子数为13NA个,故C错误;
D.标况下水是液态,不能使用气体摩尔体积,故D错误;
故选:A.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握物质的量与阿伏伽德罗常数、摩尔质量、物质的量浓度等物理量之间的转化关系是解题关键,注意气体摩尔体积的使用条件和对象,题目难度不大.

练习册系列答案
相关题目
15.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 54 g Al与足量稀硫酸反应,转移的电子数为6 NA | |
| B. | 标准状况下,1.8 g H2O所占的体积约为2.24 L | |
| C. | 物质的量浓度为0.5 mol•L-1的MgCl2溶液中,含有Cl-个数为NA | |
| D. | 1 mol铁与足量的氯气反应,失去的电子数为2 NA |
16.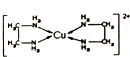 CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),其结构如图所示.则配离子[Cu(En)2]2+的配位数和该微料含有的微料间的作用力类型均正确的是( )
CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),其结构如图所示.则配离子[Cu(En)2]2+的配位数和该微料含有的微料间的作用力类型均正确的是( )
 CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),其结构如图所示.则配离子[Cu(En)2]2+的配位数和该微料含有的微料间的作用力类型均正确的是( )
CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),其结构如图所示.则配离子[Cu(En)2]2+的配位数和该微料含有的微料间的作用力类型均正确的是( )| A. | 4,配位键、极性键、非极性键 | B. | 2,极性键、非极性键、氢键 | ||
| C. | 4,离子键、配位键、氢键 | D. | 2,配位键、非极性键、极性键、氢键 |
20.下列关于物质应用的说法不正确的是( )
| A. | 用SO2漂白食品 | B. | 用硅制作太阳能电池 | ||
| C. | 工业上用氮气和氢气合成氨 | D. | 可用氢氟酸蚀刻玻璃 |
10.用 NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 5.6 g铁和足量氯气反应时,铁失去的电子数为0.2 NA | |
| B. | 22.4 L甲烷(CH4)所含的原子数为5 NA | |
| C. | 常温常压下,28 g氮气所含的原子数为2NA | |
| D. | 在20℃,1.01×105Pa时,11.2 L氧气所含的原子数为NA |
17.用下列气体和液体进行喷泉实验,最终液体一定不能充满烧瓶的是( )
| A. | CO2和NaOH溶液 | B. | SO2和NaOH溶液 | C. | NH3和H2O | D. | NO2和H2O |
8.下列叙述正确的是( )
| A. | 纯碱、烧碱均属于碱 | B. | Na2O、CaO均属于碱性氧化物 | ||
| C. | 凡能电离出H+的化合物均属于酸 | D. | 盐类物质一定含有金属离子 |