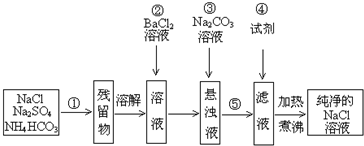
题目内容
8.通常状况下能共存,且能用碱石灰干燥的一组气体是( )| A. | H2,N2,SO2 | B. | H2,N2,O2 | C. | HCl,NO2,NH3 | D. | O2,NO2,NO |
分析 能够发生反应的气体分子之间不能共存,如氯化氢与氨气、一氧化氮与氧气等;碱石灰为碱性干燥剂,只能用于干燥碱性或者中性气体,不能干燥酸性气体,据此对各选项进行判断.
解答 解:A.H2、N2、SO2之间不发生反应,但SO2与碱石灰反应,不能够用碱石灰干燥,故A错误;
B.H2、N2、O2之间不反应,都不与碱石灰反应,可以用碱石灰干燥,故B正确;
C.NH3、HCl之间能够反应,且HCl、NO2为酸性气体,能够与碱石灰反应,不能使用碱石灰干燥氯化氢,故C错误;
D.O2、NO之间能够发生反应生成二氧化氮,一氧化氮与氧气不能共存,且不能用碱石灰干燥二氧化氮气体,故D错误;
故选B.
点评 本题考查了气体的共存与干燥,题目难度不大,注意掌握常见气体的化学性质及干燥方法,明确碱石灰为碱性干燥剂,不能干燥酸性气体,试题侧重基础知识的考查,培养了学生灵活应用基础知识的能力.

练习册系列答案
相关题目
13.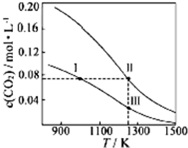 在体积均为1.0L的量恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )
在体积均为1.0L的量恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )
 在体积均为1.0L的量恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )
在体积均为1.0L的量恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1molCO2和0.2molCO2,在不同温度下反应CO2(g)+C(s)?2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上).下列说法正确的是( )| A. | 反应CO2(g)+C(s)?2CO(g)的△S>0、△H<0 | |
| B. | 体系的总压强P总:P总(状态Ⅱ)>2P总(状态Ⅰ) | |
| C. | 体系中c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ) | |
| D. | 逆反应速率V逆:V逆(状态Ⅰ)>V逆(状态Ⅲ) |
19.W、X、Y、Z是四种短周期元素,X、Y处于同一周期,X的主族序数是周期序数的2倍,Y2-、Z+、W3+的电子层结构相同,下列说法正确的是( )
| A. | 原子序数:W>X>Y>Z | B. | 原子半径:Z>W>X>Y | ||
| C. | 离子半径:W3+>Y2->Z+ | D. | 单质沸点:W>X>Y>Z |
16.下列关于实验操作或设计的说法正确的是( )
| A. | 乙酸与乙酸乙酯的混合物,可通过蒸馏或用足量饱和碳酸钠溶液洗涤后分液的方法进行分离 | |
| B. | 做金属钠和水反应实验时,切割下来的表层物质,也不能直接丢弃到废纸篓里,而应放回原试剂瓶 | |
| C. | 酸式滴定管在润洗时,可在滴定管中加入少量待装液,润洗后将溶液从滴定管的上口倒入废液缸中,重复2~3次,润洗完毕 | |
| D. | 高锰酸钾是一种常用的化学试剂,当高锰酸钾晶体结块时,应在研钵中用力研磨,以得到细小晶体,有利于加快反应或溶解的速率 |
3.现有三组混合物:①水和苯 ②汽油和柴油 ③碘和氯化钠单质溶液,正确的分离方法依次是( )
| A. | 萃取,蒸馏,分液 | B. | 分液,萃取,蒸馏 | C. | 蒸馏,萃取,分液 | D. | 分液,蒸馏,萃取 |
13.离子方程式书写正确的是( )
| A. | 铁粉加入到稀硫酸溶液中:Fe+2H+=Fe3++H2↑ | |
| B. | 氢氧化钠溶液吸收氯气:Cl2+2OH-=H2O+ClO-+Cl- | |
| C. | 稀硫酸与氢氧化钡溶液混合产生沉淀:Ba2++SO42-═BaSO4↓ | |
| D. | 氯化铁溶液中加入铁粉:Fe+Fe3+═2Fe2+ |
18.配置240mL1.84mol•L-1稀硫酸,下列操作正确的是( )
| A. | 将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,并不断搅拌至冷却 | |
| B. | 必须的定量仪器有100mL量筒、250mL容量瓶和托盘天平 | |
| C. | 量取质量分数为98%的浓硫酸(ρ=1.84g•cm-3)的体积为25.0mL | |
| D. | 先在容量瓶中加入适量水,将量好的浓硫酸注入容器瓶加入定容 |
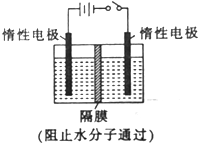 以NO2为原料可以制得新型绿色硝化剂N2O5,原理是先将NO2转化为N2O4,然后采用电解法制备N2O5,其装置如图所示.
以NO2为原料可以制得新型绿色硝化剂N2O5,原理是先将NO2转化为N2O4,然后采用电解法制备N2O5,其装置如图所示.