题目内容
17.实验室里需要纯净的溶液,但现在只有混有硫酸钠、碳酸氢铵的氯化钠.某学生设计了如下方案: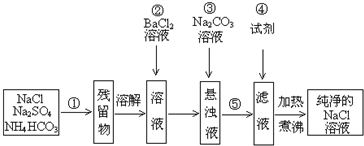
根据以上设计方案,回答下列问题:
(1)操作①和⑤的方法分别是加热、过滤;
(2)操作②是否可改为加硝酸钡溶液?为什么?否,(填是或否)理由:引入的NO3-离子无法除去.
(3)操作②后,如何判断SO42-已除尽,方法是用洁净的试管取少量的上层清夜,滴加酸化的BaCl2溶液,看是否有浑浊现.
(4)操作③的目的是除去Ba2+;
(5)操作④加的试剂是盐酸;发生反应的离子方程式为:CO32-+2H+=CO2↑+H2O.
分析 由分离流程可知,①为加热,碳酸氢铵分解生成水、氨气、二氧化碳,残留物为NaCl、硫酸钠,溶解后加氯化钡除去硫酸根离子,再加碳酸钠除去钡离子,过滤除去沉淀硫酸钡、碳酸钡,向滤液中加盐酸,与碳酸钠反应生成NaCl,最后蒸发得到纯净的NaCl,以此来解答.
解答 解:由分离流程可知,①为加热,碳酸氢铵分解生成水、氨气、二氧化碳,残留物为NaCl、硫酸钠,溶解后加氯化钡除去硫酸根离子,再加碳酸钠除去钡离子,过滤除去沉淀硫酸钡、碳酸钡,向滤液中加盐酸,与碳酸钠反应生成NaCl,最后蒸发得到纯净的NaCl,
(1)由上述分析可知,①为加热,⑤为过滤,故答案为:加热;过滤;
(2)操作②不能改为加硝酸钡溶液,引入的NO3-离子无法除去,故答案为:否;引入的NO3-离子无法除去;
(3)判断SO42-已除尽的方法为用洁净的试管取少量的上层清夜,滴加酸化的BaCl2溶液,看是否有浑浊现象,故答案为:用洁净的试管取少量的上层清夜,滴加酸化的BaCl2溶液,看是否有浑浊现;
(4)操作③的目的是除去Ba2+,故答案为:除去Ba2+;
(5)操作④加的试剂是盐酸,发生的离子反应为CO32-+2H+=CO2↑+H2O,故答案为:盐酸;CO32-+2H+=CO2↑+H2O.
点评 本题考查混合物分离提纯的综合应用,为高频考点,把握流程中的反应及混合物分离方法为解答的关键,侧重分析与实验能力的综合考查,题目难度不大.

练习册系列答案
 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案 互动课堂系列答案
互动课堂系列答案
相关题目
7.下列离子能大量共存的是( )
| A. | 含大量 H+的溶液中:CrO42-、Cl-、N03-、Na+ | |
| B. | 含大量 A102-的溶液中:Na+、K+、NO3-、HCO3- | |
| C. | 含大量 Al3+的溶液中:K+、Na+、NO3-、Cl0- | |
| D. | 含大量 CH3COO- 的溶液中:NH4+、Cl-、F-、K+ |
8.通常状况下能共存,且能用碱石灰干燥的一组气体是( )
| A. | H2,N2,SO2 | B. | H2,N2,O2 | C. | HCl,NO2,NH3 | D. | O2,NO2,NO |
5.亚磷酸(H3PO3)是二元弱酸,且具有较强还原性.下列说法正确的是( )
| A. | Na2HPO3溶液显碱性,说明HPO32-的电离程度大于水解程度 | |
| B. | 25℃时,将0.1 mol•L-1的亚磷酸溶液加水稀释后,n(H+)与n(OH-)的乘积不变 | |
| C. | 利用H3PO3进行化学镀银,当参加反应的$\frac{n(A{g}^{+})}{n({H}_{3}P{O}_{3})}$=2时,氧化产物为H3PO4 | |
| D. | NaH2PO3溶液显酸性,其溶液中存在的粒子浓度关系:c(H2PO3-)>c(HPO32-)>c(H3PO3)>c(H+)>c(OH-) |
12.可逆反应CO(g)+H2O(g)$\stackrel{△}{?}$ CO2(g)+H2(g),达到平衡后,有关化学反应限度的说法正确的是( )
| A. | V正=0 | B. | V逆=0 | C. | V正=V逆≠0 | D. | V正=V逆=0 |
2.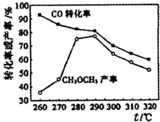 研究者在某条件下探究制备二甲醚反应:2CO(g)+4H2(g)?CH3 OCH3(g)+H2 O(g)△H,测定结果如图所示.下列判断错误的是( )
研究者在某条件下探究制备二甲醚反应:2CO(g)+4H2(g)?CH3 OCH3(g)+H2 O(g)△H,测定结果如图所示.下列判断错误的是( )
 研究者在某条件下探究制备二甲醚反应:2CO(g)+4H2(g)?CH3 OCH3(g)+H2 O(g)△H,测定结果如图所示.下列判断错误的是( )
研究者在某条件下探究制备二甲醚反应:2CO(g)+4H2(g)?CH3 OCH3(g)+H2 O(g)△H,测定结果如图所示.下列判断错误的是( )| A. | △H<0 | |
| B. | 该反应伴随有副反应的发生 | |
| C. | 制备二甲醚的适宜温度为280~290℃ | |
| D. | 加入催化剂可以提高CH3 OCH3的产率 |
7.二氧化硫能使溴水褪色,说明二氧化硫具有( )
| A. | 还原性 | B. | 氧化性 | C. | 漂白性 | D. | 酸性 |
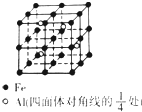 某宝石的主要成分是Al2O3,其中混有少量Mg、Ti、Fe等杂质而使其呈蓝色.
某宝石的主要成分是Al2O3,其中混有少量Mg、Ti、Fe等杂质而使其呈蓝色.