题目内容
13.下列反应中,硫表现出氧化性的是( )| A. | 稀硫酸与Zn粒反应 | B. | SO2与O2反应 | ||
| C. | 浓硫酸与铜反应 | D. | SO3与水反应 |
分析 硫表现出氧化性,元素化合价应降低,在反应中得到电子,以此解答该题.
解答 解:A.硫元素化合价没有发生变化,故A错误;
B.反应生成三氧化硫,S元素化合价升高,被氧化,表现还原性,故B错误;
C.反应生成二氧化硫,硫元素化合价降低,表现氧化性,故C正确;
D.生成硫酸,元素化合价没有发生变化,故D错误.
故选C.
点评 本题考查氧化还原反应,为高考常见题型,侧重于学生的分析能力的考查,注意从元素化合价变化的角度认识氧化还原反应的概念和物质具有的性质,难度不大.

练习册系列答案
 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
4.水的沸点为100℃,硫化氢的分子结构跟水相似,但它的沸点却很低,是-60.7℃,引起这种差异的主要原因是( )
| A. | 范德华力 | B. | 共价键 | C. | 氢键 | D. | 相对分子质量 |
1.用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是( )
| 选项 | 操作及现象 | 溶液 |
| A | 通入CO2,溶液不变浑浊.先通入CO2再通入氨气,溶液变浑浊 | CaCl2溶液 |
| B | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失. | Na2SiO3溶液 |
| C | 通入CO2,溶液变浑浊.再加入品红溶液,红色褪去. | Ca(ClO)2溶液 |
| D | 通入CO2,溶液变浑浊.继续通CO2至过量,浑浊消失.再加入足量NaOH溶液,又变浑浊. | Ca(OH)2溶液 |
| A. | A | B. | B | C. | C | D. | D |
5.下列说法中正确的是( )
| A. | 1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L | |
| B. | 从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol/L | |
| C. | 配制500 mL 0.5 mol/L的CuSO4溶液,需62.5 g胆矾 | |
| D. | 中和100 mL 1 mol/L的H2SO4溶液,需NaOH 4 g |
2.如图是化学实验常用装置之一,若气体从右管进入,可用来收集的气体是( )
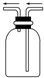

| A. | NO | B. | NO2 | C. | CO | D. | SO2 |
3.下列物质中前者是混合物,后者是纯净物的是( )
| A. | 铜绿、氧化镁 | B. | 空气、石灰水 | C. | 矿泉水、水煤气 | D. | 海水、胆矾 |