题目内容
18.亚硝酸钠(NaNO2)是工业盐,常被误食引起中毒,已知它能氢碘酸(HI)发生反应,生成NO和碘单质.(1)上述反应中氧化剂是NaNO2,发生氧化反应的物质的是HI;
(2)根据上述反应,可用试纸和生活中常见的物质进行检验,以鉴别NaNO2和食盐,可选用的物质的有:①自来水②淀粉碘化钾试纸③淀粉④白糖⑤食醋⑥酒精.进行实验时,必须选用的是②⑤.
分析 (1)2NaNO2+4HI=I2+2NO↑+2H2O+2NaI该反应中N元素的化合价降低,I元素的化合价升高;
(2)鉴别亚硝酸钠和食盐,由2NaNO2+4HI=I2+2NO↑+2H2O+2NaI可知,若生成碘单质使淀粉变蓝可检验亚硝酸钠,以此来解答.
解答 解:(1)2NaNO2+4HI=I2+2NO↑+2H2O+2NaI,N元素的化合价降低,氧化剂为NaNO2,I元素的化合价升高,则HI发生氧化反应,
故答案为:NaNO2;HI;
(2)鉴别亚硝酸钠和食盐,由2NaNO2+4HI=I2+2NO↑+2H2O+2NaI可知,生成碘单质使淀粉变蓝可检验亚硝酸钠,则选择试剂为②⑤,且与食盐不反应,现象不同,能鉴别,
故答案为:②⑤.
点评 本题考查氧化还原反应和离子反应,把握反应中元素的化合价变化及离子反应的书写方法为解答的关键,侧重氧化还原反应中基本概念及物质鉴别的考查,题目难度不大.

练习册系列答案
相关题目
6.下列分子中,键角最大的是( )
| A. | H2S | B. | H2O | C. | CCl4 | D. | NH3 |
13.下列反应中,硫表现出氧化性的是( )
| A. | 稀硫酸与Zn粒反应 | B. | SO2与O2反应 | ||
| C. | 浓硫酸与铜反应 | D. | SO3与水反应 |
3.下列选项中最后的物质是要制取的物质,其中不可能得到的是( )
| A. | CaCO3$\stackrel{高温}{→}$CaO$\stackrel{H_{2}O}{→}$Ca(OH)2$→_{过滤}^{Na_{2}CO_{3}}$NaOH溶液 | |
| B. | Cu$→_{△}^{O_{2}}$CuO$→_{△}^{H_{2}SO_{4}}$CuSO4溶液$→_{过滤}^{NaOH溶液}$Cu(OH)2沉淀 | |
| C. | KMnO4$\stackrel{△}{→}$O2$\stackrel{点燃S}{→}$SO3$\stackrel{H_{2}O}{→}$H2SO4溶液 | |
| D. | BaCO3$\stackrel{盐酸}{→}$BaCl2溶液$\stackrel{通入H_{2}SO_{4}}{→}$BaSO4沉淀 |
10.下列有关铁的叙述正确的是( )
| A. | 在空气中,铁丝如同镁条一样能被点燃,并发出耀眼的强光 | |
| B. | 铁是地壳里含量最多的金属元素 | |
| C. | 铁在高温下与水蒸气反应生成氢气和四氧化三铁 | |
| D. | 铁能与稀盐酸、浓硫酸、碳酸等酸反应生成氢气和亚铁盐 |
7.限一种试剂,经过一次性实验就能鉴别Na2CO3、(NH4)2SO4、NH4Cl、KNO3溶液,应选用( )
| A. | AgNO3 溶液 | B. | NaOH溶液 | C. | Ba(OH)2溶液 | D. | 盐酸 |
8.下列反应中,不属于置换反应的是( )
| A. | Fe+CuSO4═FeSO4+Cu | B. | CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | ||
| C. | C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ | D. | Fe+2HCl═FeCl2+H2↑ |
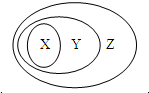 用下图表示的一些物质或概念间的从属关系中不正确的是( )
用下图表示的一些物质或概念间的从属关系中不正确的是( )