题目内容
4.水的沸点为100℃,硫化氢的分子结构跟水相似,但它的沸点却很低,是-60.7℃,引起这种差异的主要原因是( )| A. | 范德华力 | B. | 共价键 | C. | 氢键 | D. | 相对分子质量 |
分析 H2O,HF,NH3中因为含有氢键,所以其沸点高于同族其他元素的氢化物.
解答 解:H2O与H2S都属于分子晶体,H2O分子间可以形成氢键,H2S只含有范德华力,氢键的作用力大于范德华力,所以水的沸点高于H2S的沸点,
故选C.
点评 本题考查了氢键对物质熔沸点的影响,题目难度不大,氢键为高考中的高频考点,H2O,HF,NH3中因为含有氢键,所以其沸点高于同族其他元素的氢化物.

练习册系列答案
相关题目
13.向Cr2(SO4)3水溶液中,加入NaOH溶液,当pH=4.6时,开始出现Cr(OH)3沉淀,随着碱性增强,沉淀增多;但当[OH-1]大于0.1mol•L-1时,沉淀消失,出现亮绿色的亚铬酸根离子(CrO2-).平衡关系如下: ,向50mL0.05mol•L-1的Cr2(SO4)3溶液中,加入1.0mol•L-1NaOH溶液50mL,反应后观察到现象是( )
,向50mL0.05mol•L-1的Cr2(SO4)3溶液中,加入1.0mol•L-1NaOH溶液50mL,反应后观察到现象是( )
 ,向50mL0.05mol•L-1的Cr2(SO4)3溶液中,加入1.0mol•L-1NaOH溶液50mL,反应后观察到现象是( )
,向50mL0.05mol•L-1的Cr2(SO4)3溶液中,加入1.0mol•L-1NaOH溶液50mL,反应后观察到现象是( )| A. | .紫色 | B. | .亮绿色 | C. | 有灰绿色沉淀 | D. | .无法判断 |
19.用铝箔包装0.1mol金属钠,用针扎出一些小孔,放入水中,完全反应后,用排水集气法收集产生的气体,则收集到的气体为(标准状况)( )
| A. | O2和H2的混合气体 | B. | 1.12L H2 | ||
| C. | 大于1.12L H2 | D. | 小于1.12L气体 |
13.下列反应中,硫表现出氧化性的是( )
| A. | 稀硫酸与Zn粒反应 | B. | SO2与O2反应 | ||
| C. | 浓硫酸与铜反应 | D. | SO3与水反应 |
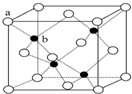 已知A、B、C、D、E、F、G为前四周期七种元素且原子序数依次增大,其中A的基态原子中没有成对电子,B的基态原子中有6种不同运动状态的电子,C原子核外成对电子数比未成对电子数多1,其氢化物常用作制冷剂,D原子中有2个未成对电子,E基态原子在同周期中原子半径最大,F原子价电子排布为nsn-1nPn+1,G基态原子核外所有轨道都处于全满状态且属ds区的元素.
已知A、B、C、D、E、F、G为前四周期七种元素且原子序数依次增大,其中A的基态原子中没有成对电子,B的基态原子中有6种不同运动状态的电子,C原子核外成对电子数比未成对电子数多1,其氢化物常用作制冷剂,D原子中有2个未成对电子,E基态原子在同周期中原子半径最大,F原子价电子排布为nsn-1nPn+1,G基态原子核外所有轨道都处于全满状态且属ds区的元素.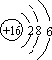 ;化合物B2A4的电子式为
;化合物B2A4的电子式为 .
. .
.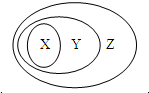 用下图表示的一些物质或概念间的从属关系中不正确的是( )
用下图表示的一些物质或概念间的从属关系中不正确的是( )