题目内容
8.有机化合物A的分子量为100,其中碳的质量分数为60%,氢的质量分数为8%,其余为氧,那么A的分子式是( )| A. | C7H16 | B. | C5H8O2 | C. | C4H4O3 | D. | C6H12O |
分析 根据化合物A的分子量及C、H元素的质量分数可以分别计算出A分子中含有的C、H原子数,再结合A的分子量可以计算出A中含有的O原子数,从而确定其分子式.
解答 解:有机化合物A的分子量为100,其中碳的质量分数为60%,氢的质量分数为8%,
则A中含有C、H原子数为:N(C)=$\frac{100×60%}{12}$=5、N(H)=$\frac{100×8%}{1}$=8,
A分子中含有氧原子数为:N(O)=$\frac{100-12×5-1×8}{16}$=2,
所以有机化合物A的分子式为:C5H8O2,
故选B.
点评 本题考查了有机物分子式的确定,题目难度不大,试题侧重基础知识的考查,明确质量守恒定律在确定有机物分子式中的应用方法,试题培养了学生灵活应用基础知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.向一密闭容器中充入1mol N2和3mol H2,在一定条件下发生反应(N2+3H2?2NH3).下列有关说法不正确的是( )
| A. | 达到化学平衡时,N2、H2和NH3的物质的量之比为1:3:2 | |
| B. | 达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化 | |
| C. | 达到化学平衡时,N2不能完全转化为NH3 | |
| D. | 达到化学平衡时,容器中气体的总压强不再发生变化 |
5.某实验小组的同学想用碳酸钠溶液与饱和石灰水反应来制取氢氧化钠.
(1)该复分解反应发生的理由是氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,有沉淀生成,该反应能够发生;
(2)有人提出:实验时没有注意药品的用量,所得到的氢氧化钠溶液可能不纯.
猜想一:只含NaOH;
猜想二:含有NaOH和Na2CO3;
猜想三:含有NaOH和Ca(OH)2.
(3)为了验证猜想一成立,请你根据可选用的试剂,完成实验设计方案并填写以下表格.可选试剂:NaCl溶液、稀盐酸、Na2CO3溶液
(1)该复分解反应发生的理由是氢氧化钙与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,有沉淀生成,该反应能够发生;
(2)有人提出:实验时没有注意药品的用量,所得到的氢氧化钠溶液可能不纯.
猜想一:只含NaOH;
猜想二:含有NaOH和Na2CO3;
猜想三:含有NaOH和Ca(OH)2.
(3)为了验证猜想一成立,请你根据可选用的试剂,完成实验设计方案并填写以下表格.可选试剂:NaCl溶液、稀盐酸、Na2CO3溶液
| 实验步骤 | 实验操作 | 预期现象及结论 |
| 1 | 取少量所得溶液于试管中, 再滴入几滴稀盐酸 | 若无气泡产生,证明原溶液中不含有Na2CO3 |
| 2 | 另取少量所得溶液于试管中, 再滴入几滴Na2CO3溶液 | 若无沉淀产生,结合步骤1,猜想一成立. |
3.下列所有元素组合,既可以形成离子化合物,又可形成共价化合物的一组是( )
| A. | H、C、O、K | B. | H、N、O | C. | H、O、S | D. | H、O、S、Na |
20.下列配合物的水溶液中加入硝酸银不能生成沉淀的是( )
| A. | [Co(NH3)4 Cl2]Cl | B. | [Cu(NH3)4]Cl2 | C. | [Co(NH3)6]Cl3 | D. | [Co(NH3)3 Cl3] |
17.用a、b、c、d四种金属进行如下图所示的实验,部分反应现象如下表所示,由此判断四种金属的活动性由强到弱的顺序是( )
| 实验装置 | 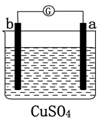 | 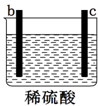 | 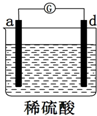 |
| 部分实验现象 | a极质量减少b极质量增加 | b极有气体产生c极无变化 | 电流从a极流向d极 |
| A. | abcd | B. | bcda | C. | dabc | D. | abdc |

 .
.