题目内容
(7分)氮元素可以形成多种化合物。
(1)基态氮原子的价电子轨道表示式是 。
(2)已知尿素的结构式为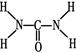 ,则尿素分子中C和N原子的杂化方式分别是、。
,则尿素分子中C和N原子的杂化方式分别是、。
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被—NH2(氨基)取代形成的另一种氮化物。
①NH3分子的空间构型是;
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)=3N2(g)+4H2O(g)△H=-1038.7kJ·mol-1
当肼燃烧放出519.35kJ热量时,形成的π键有mol。
(1) (2分)(2)sp2(1分)sp3(1分)
(2分)(2)sp2(1分)sp3(1分)
(3)①三角锥形(1分)②3(2分)
解析试题分析:(1)氮元素的核外电子数是7个,则根据核外电子排布规律可知基态氮原子的价电子轨道表示式是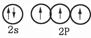 。
。
(2)根据尿素的结构简式可知,分子中氮元素全部形成单键,因此是sp3杂化;碳元素形成2个单键,1个双键,因此是sp2杂化。
(3)①氨气分子中氮原子的价层电子对数=4,其中有一对孤对电子,所以氨气是三角锥形。
②当肼燃烧放出519.35kJ热量时,根据热化学方程式可知生成氮气的物质的量是 ×3=1.5mol。氮气分子中含有2个π键,则π键的物质的量是3mol。
×3=1.5mol。氮气分子中含有2个π键,则π键的物质的量是3mol。
考点:考查核外电子排布、杂化轨道、反应热以及共价键计算等

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列分子中,所有原子都满足最外层8电子稳定结构的是( )
| A.光气(COCl2) | B.六氟化硫(SF6) |
| C.三氟化硼(BF3) | D.五氯化磷(PCl5) |
(9分)下表为元素周期表的一部分,a、b、c……为部分元素。回答下列问题:
| a | | | |||||||||||||||
| | | | | f | | h | i | | |||||||||
| | b | | e | | | | j | | |||||||||
| c | | | | | | | | d | | | | | g | | | k | |
| | | | | | | | | | | | | | | | | l | |
(2)请写出上述元素k的核外电子排布式 ;
(3)b、e、j三种元素的电负性由大到小的顺序 (写元素符号);此三种元素的第一电离能由大到小的顺序 (写元素符号);
(4)g、e两种元素的最高价氧化物对应的水合物的化学性质相似,请写出e元素最高价氧化物对应的水化物与a、c、h三种元素形成的化合物反应的离子方程式 ;
(5)j、k、l三种元素之间能以原子个数比1∶1两两形成互化物,这些互化物的性质类似于这些元素单质的性质。请写出k、l的互化物的电子式 ,它是由 键形成的 化合物(填“离子”或“共价”)。
(14分)下面是元素周期表的一部分。据A至H在周期表中位置,请回答下列问题:
| A | | | |||||||||||||||
| | | | | | E | | G | | |||||||||
| B | C | D | | | F | H | | ||||||||||
| | | | | | | | | | | | | | | | | | |
以下请用元素符号或化学式填空:
(2)原子半径最大的是 , A分别与E、F、G、H形成的化合物中,最稳定的化合物是 。
(3)最高价氧化物是两性氧化物的是 ,最高价氧化物对应的水化物碱性最强的是 ,最高价氧化物对应水化物的酸性最强的是 。
(4)C与H形成的化合物中含有 (填“共价”或“离子”)键;用电子式表示C、H形成化合物的过程 。
(11分)下表是元素周期表短周期的一部分
| ① | | | ||||||
| | | | | ② | ③ | | ④ | |
| | ⑤ | ⑥ | ⑦ | | | | | |
(2)可作为半导体材料的是 (写元素符号)。
(3)表中元素⑥的原子结构示意图为 。
(4)④与⑤形成的常见化合物的化学键的类型为 ,该化合物的电子式为 。
(5)表中元素①、②、③、⑤、⑦中,原子半径由大到小的顺序是 (填数字序号)
(6)表中元素③、⑥它们最高价氧化物的水化物相互反应的离子方程式为 。
 [Cu(NH3)3CO]Ac
[Cu(NH3)3CO]Ac