题目内容
(本题共12分)
合成氨工艺的一个重要工序是铜洗,其目的是用铜液[醋酸二氨合铜(I)、氨水]吸收在生产过程中产生的CO和CO2等气体。铜液吸收CO的反应是放热反应,其反应方程式为:
Cu(NH3)2Ac+CO+NH3 [Cu(NH3)3CO]Ac
[Cu(NH3)3CO]Ac
完成下列填空:
(1)如果要提高上述反应的反应速率,可以采取的措施是_________。(选填编号)
a.减压 b.增加NH3的浓度 c.升温 d.及时移走产物
(2)铜液中的氨可吸收二氧化碳,写出该反应的化学方程式。
_________________________________________
(3)简述铜液吸收CO及铜液再生的操作步骤(注明吸收和再生的条件)。
__________________________________________
(4)铜液的组成元素中,短周期元素原子半径从大到小的排列顺序为____________________。其中氮元素原子最外层电子排布的轨道表达式是_________________________。通过比较_____________可判断氮、磷两种非金属元素的非金属性强弱。
(5)已知CS2与CO2分子结构相似,CS2的电子式是____________。CS2熔点高于CO2,其原因是__________。
(1)bc (2)2NH3+CO2+H2O→(NH4)2CO3、(NH4)2CO3+CO2+H2O→2NH4HCO
(3)①低温加压下吸收CO;②然后将铜液洗涤转移至另一容器中;③高温低压下释放CO,然后将铜洗液循环利用。
(4)C>N>O>H;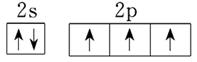 ;NH3和PH3的稳定性
;NH3和PH3的稳定性
(5)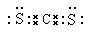 ;CS2和CO2都是分子晶体,CS2的相对分子质量大,分子间作用力大。
;CS2和CO2都是分子晶体,CS2的相对分子质量大,分子间作用力大。
解析试题分析:(1)降低压强,反应速率减小,a不正确;增加NH3的浓度或升高温度,反应速率均增大bc正确;及时移走产物,即降低生成物浓度,反应速率也减小,d不正确,答案选bc。
(2)氨气是碱性气体,CO2是酸性气体,二者反应的化学方程式为2NH3+CO2+H2O→(NH4)2CO3、(NH4)2CO3+CO2+H2O→2NH4HCO3。
(3)根据Cu(NH3)2Ac+CO+NH3 [Cu(NH3)3CO]Ac可知,该反应是体积减小的放热的可逆反应,因此吸收CO的适宜条件是低温加压下吸收CO。若要再生,则只需要将铜液洗涤转移至另一容器中;然后高温低压下释放CO,最后将铜洗液循环利用即可。
[Cu(NH3)3CO]Ac可知,该反应是体积减小的放热的可逆反应,因此吸收CO的适宜条件是低温加压下吸收CO。若要再生,则只需要将铜液洗涤转移至另一容器中;然后高温低压下释放CO,最后将铜洗液循环利用即可。
(4)铜液的组成元素中属于短周期元素的是H、C、N、O,同周期自左向右原子半径逐渐减小,同主族自上而下原子半径逐渐增大,则四种元素的原子半径大小顺序是C>N>O>H;氮元素原子最外层有4个电子,根据核外电子排布规律可知,最外层电子排布的轨道表达式是 。非金属性越强,氢化物的稳定性越强,因此可通过比较NH3和PH3的稳定性判断氮、磷两种非金属元素的非金属性强弱。
。非金属性越强,氢化物的稳定性越强,因此可通过比较NH3和PH3的稳定性判断氮、磷两种非金属元素的非金属性强弱。
(5)已知CS2与CO2分子结构相似,则根据CO2的电子式可得CS2的电子式是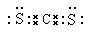 。CS2和CO2都是分子晶体,CS2的相对分子质量大,分子间作用力大,因此CS2熔点高于CO2。
。CS2和CO2都是分子晶体,CS2的相对分子质量大,分子间作用力大,因此CS2熔点高于CO2。
考点:考查外界条件对反应速率和平衡状态的影响、核外电子排布、元素周期律、晶体性质以及电子式

 阅读快车系列答案
阅读快车系列答案(9分)4种相邻的主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。回答下列问题:
| | | m | n |
| x | y | | |
(2)m、n、y三种元素最高价氧化物的水化物中,酸性最强的是______,碱性最强的是______.(填化学式)
(3)气体分子(mn)2的电子式为_______,(mn)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式是_____________________________。
(9分)元素周期律是指导我们学习元素及其化合物知识的重要工具。已知氧族元素(不含Po)的部分知识如下表所示,
| 元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | | 450 |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 元素主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
(1)单质硒的熔点范围可能是________________。
(2)元素碲的主要化合价可能有________________。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是________________(用化学式表示)。
(4)氢硒酸有较强的__________(填“氧化性”或“还原性”),因此露置在空气中长期保存易变质,其可能发生反应的化学方程式为_________________________________。
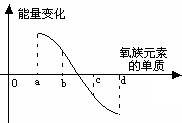
(5)下图所示为氧族元素单质与H2反应过程中的能量变化示意图,其中a、b、c、d分别表示氧族元素中某一元素的单质,纵坐标为相同物质的量的单质与H2反应过程中的能量变化(能量变化>0表示放热,能量变化<0表示吸热)。则:b代表___________ _____, d代表 (均写单质名称)。
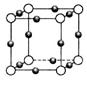
某金属(A)在TK以下晶体的基本结构单元如左下图所示,T K以上转变为右下图所示结构的基本结构单元,在两种晶体中最邻近的A原子间距离相同

(1)在T K以下的纯A晶体中,与A原子等距离且最近的A原子数为______个;在T K以上的纯A晶体中,与A原子等距离且最近的A原子数为___________;
(2)纯A晶体在晶型转变前后,二者基本结构单元的边长之比为(TK以上与TK以下之比)___________。
(3)左上图的的堆积方式为 , TK以下经测定其结构和性质参数如下表所示
| 金属 | 相对原子质量 | 分区 | 原子半径/pm | 密度/g·㎝-3 | 原子化热/kJ·mol-1 |
| Na | 22.99 | s区 | 186 | 0.960 | 108.4 |
| A | 60.20 | d区 | r | 7.407 | 7735 |
。
(已知
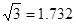 ,7.407≈
,7.407≈ ,1pm=10
,1pm=10 m)
m) (12分)甲同学拟通过实验探究同主族元素性质的递变规律,以及影响化学反应速率的因素。其设计的实验方案如下,请你帮他填写完整,并做出评价。
实验室提供的试剂:锌块、锌粉、铁条、铁粉、铜条、NaBr溶液、NaI溶液、新制的氯水、1mol/L盐酸、3mol/L的盐酸
(1)探究同主族元素性质的递变规律
①写出下列实验报告中的实验现象和离子方程式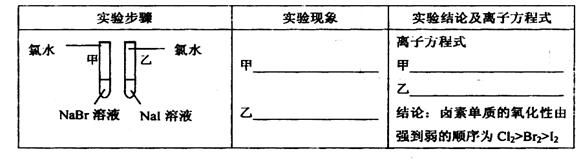
②【评价】甲同学设计的实验方案的合理性是___________(填序号)
A. 非常合理 B. 部分合理 C. 完全不合理
③【补充和完善】上一题②中若选A,则此项不用再作答,若选B或C,则完成实验还需要的试剂是___________。
(2)探究影响化学反应速率的因素
| 实验步骤 | 实验现象 | 实验依据和结论 |
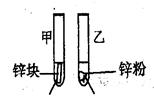 3mL1mol/L 3mL3mol/L 盐酸 盐酸 (金属质量相同,盐酸均过量) | 均有气体生成,锌粉先消失,锌块后消失 | 因为乙试管中的反应更快,所以反应物浓度越大,反应速率越快。 |
(3)请你利用原电池原理,设计实验,比较铜和铁的金属活动性。画出实验装置图,标出正负极、电子流动方向,写出电极反应式。
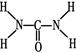 ,则尿素分子中C和N原子的杂化方式分别是、。
,则尿素分子中C和N原子的杂化方式分别是、。


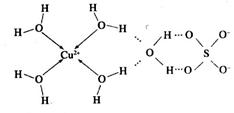
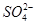 的空间构型为_________,H2O中O原子的杂化方式为____________。
的空间构型为_________,H2O中O原子的杂化方式为____________。 配离子。已知
配离子。已知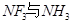 的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是____________________________。
的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是____________________________。 N形成的晶体结构如图所示,N3-的配位数是________。设晶胞边长为a cm,密度为b g/cm3,则阿伏加德罗常数可表示为___________(用含a、b的式子表示)。
N形成的晶体结构如图所示,N3-的配位数是________。设晶胞边长为a cm,密度为b g/cm3,则阿伏加德罗常数可表示为___________(用含a、b的式子表示)。