题目内容
【题目】氨气和氨水在工农业生产中均有重要应用。
(1)工业合成氨反应的化学方程式是_________。
(2)实验室常加热熟石灰[主要成分是Ca(OH)2]和氯化铵混合固体制取氨气,写出反应的化学方程式___________。
(3)如图所示,向表面皿中的NaOH固体滴几滴浓氨水,迅速盖上盖,观察现象。
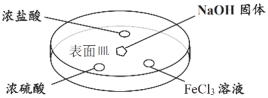
①___________液滴上方会出现白烟(填序号)
A.浓盐酸 B.浓硫酸 C.FeCl3溶液
②一段时间后浓硫酸的液滴中有白色固体,生成该白色固体的化学方程式是_______。
③FeCl3液滴中出现的现象是___________,发生反应的离子方程式是_________。
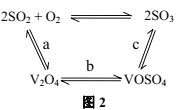
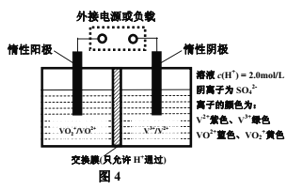
(4)利用氨水可以将大气污染物SO2吸收并生产氮肥,原理如图所示:
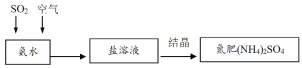
分析上述生产原理,在下列表格中填写该生产过程中利用的SO2的化学性质并进行理论论证
SO2的化学性质 | 理论论证 |
______ | ______ |
______ | ______ |
【答案】N2+3H2 2NH3 Ca(OH)2+2NH4Cl
2NH3 Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O A H2SO4+2NH3=(NH4)2SO4 黄色液滴中产生红褐色沉淀 Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+ 与氨水反应生成铵盐 SO2是酸性氧化物 还原性,被氧气氧化 SO2中S为+4价,可升至+6价,具有还原性,可以与氧气反应生成硫酸盐
CaCl2+2NH3↑+2H2O A H2SO4+2NH3=(NH4)2SO4 黄色液滴中产生红褐色沉淀 Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+ 与氨水反应生成铵盐 SO2是酸性氧化物 还原性,被氧气氧化 SO2中S为+4价,可升至+6价,具有还原性,可以与氧气反应生成硫酸盐
【解析】
(1)工业合成氨,是在高温、高压、并有催化剂作用的条件下,N2与H2反应生成NH3。
(2)熟石灰[主要成分是Ca(OH)2]和氯化铵混合加热,可生成CaCl2和氨气。
(3)氨气与浓盐酸挥发出的HCl气体反应,生成NH4Cl,产生白烟;氨气与浓硫酸反应生成硫酸铵,但看不到明显的现象;氨气与NaOH固体不反应;氨气溶于FeCl3溶液中,生成Fe(OH)3沉淀和NH4Cl。
①由以上分析,可确定哪种液滴上方会出现白烟。
②由以上分析,可确定一段时间后浓硫酸的液滴中白色固体的成分。
③FeCl3液滴中生成Fe(OH)3沉淀。
(4)氨水中通入SO2,发生反应生成(NH4)2SO3;通入空气后,(NH4)2SO3被氧化生成(NH4)2SO4。
(1)工业合成氨,是在高温、高压、并有催化剂作用的条件下,N2与H2反应生成NH3,反应的化学方程式为N2+3H2![]() 2NH3。答案为:N2+3H2
2NH3。答案为:N2+3H2![]() 2NH3;
2NH3;
(2)熟石灰[主要成分是Ca(OH)2]和氯化铵混合加热,可生成CaCl2和氨气,反应的方程式为2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O。答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O。答案为:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
(3) ①A.浓盐酸为挥发性酸,挥发出的HCl气体与氨气结合成NH4Cl,产生白烟,A符合题意;
B.浓硫酸为不挥发性酸,与NH3反应生成硫酸铵,但不产生现象,B不合题意;
C.FeCl3溶液与溶解在其中的氨反应,生成红褐色Fe(OH)3沉淀和NH4Cl,C不合题意;
故选A;
②一段时间后浓硫酸的液滴中有白色固体(NH4)2SO4,生成(NH4)2SO4的化学方程式是H2SO4+2NH3=(NH4)2SO4。答案为:H2SO4+2NH3=(NH4)2SO4;
③FeCl3液滴中生成红褐色Fe(OH)3沉淀和NH4Cl,出现的现象是黄色液滴中产生红褐色沉淀,发生反应的离子方程式是Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+。答案为:黄色液滴中产生红褐色沉淀;Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+;
(4)氨水中通入SO2,发生反应生成(NH4)2SO3;通入空气后,(NH4)2SO3被氧化生成(NH4)2SO4。
SO2的化学性质 | 理论论证 |
与氨水反应生成铵盐 | SO2是酸性氧化物 |
还原性,被氧气氧化 | SO2中S为+4价,可升至+6价,具有还原性,可以与氧气反应生成硫酸盐 |
答案为:与氨水反应生成铵盐;SO2是酸性氧化物;还原性,被氧气氧化; SO2中S为+4价,可升至+6价,具有还原性,可以与氧气反应生成硫酸盐。

【题目】溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据:
苯 | 溴 | 溴苯 | |
密度/g·cm﹣3 | 0.88 | 3.10 | 1.50 |
沸点/℃ | 80 | 59 | 156 |
水中溶解度 | 微溶 | 微溶 | 微溶 |
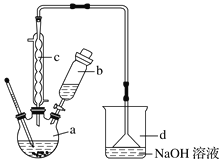
按下列合成步骤回答问题:
(1)在a中加入15mL无水苯和少量铁屑,在b中小心加入4.0mL液态溴,向a中滴入几滴溴,有白色烟雾产生,是因为生成了_______气体,继续滴加液溴滴完。铁屑的作用是___________;a中发生的化学反应方程式______________________。
(2)液溴滴完后,经过下列步骤分离提纯:
①向a中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤。NaOH溶液洗涤的作用是____;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_______;
(3)经以上分离操作后,粗溴苯中还含有的主要杂质为______,要进一步提纯,下列操作中必须的是______(填入正确选项前的字母);
A.重结晶B.过滤C.蒸馏D.萃取
(4)在该实验中,a的容积最适合的是_______(填入正确选项前的字母)。
A.25mL B.50mL C.250mL D.500mL