��Ŀ����
����Ŀ���ж�����ļ��źʹ����ǹ�ҵ�����е���Ҫ���⡣
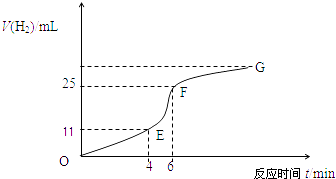
��1��Na2CO3��Һ������β��SO2,��Ӧ��������Һ��ɱ仯����ͼ��

��SO2��������________ (ѡ���������������Ǽ�����) ���ӣ����Ϸ�Ӧ_____(ѡ������������������) ˵��S��C����Ԫ�صķǽ�����ǿ����
��A�㷴Ӧ�����ӷ���ʽ��_____��
��2������������ϡȼ����ϵͳ��Ҫ����ԭ���Ƿ�������ϡȼ��ȼ�����½�����У�β���е�NOx�ڴ����Ϸ�Ӧ�ѳ����乤��ԭ��ʾ��ͼ����:

����֪Ba(NO3)2�ֽ���ﺬ���������壬����ͼ��Ϣ��д��Ba(NO3)2�ֽⷴӦ�Ļ�ѧ����ʽ_______��
������˵����ȷ����__________
A.ϡȼ���̵�Ŀ���ǹ̵�
B.�����������У�Pt��BaO���ɿ�������
C.����β���������������еĵ�������ȿ����γɹ⻯ѧ����
D.��ȼ�����У�NO2��CO��Ӧ����������ͻ�ԭ��������ʵ���֮��Ϊ1:1
��ʵ������ÿǧ��CxHy (��Һ��C8H18Ϊ��) ��O2�г��ȼ������Һ̬ˮ���ų�4.78��104kJ������д��C8H18ȼ���ȵ��Ȼ�ѧ��Ӧ����ʽ______________��
��3�����ؿ�����ʪ�������ѵ����գ��䷴Ӧԭ��Ϊ:
NO+NO2+ H2O =2HNO2 2HNO2+CO(NH2)2=2N2��+CO2��+3H2O��
����ͼ�����غ������ѵ�Ч�ʵ�Ӱ�죬�Ӿ��������Ͽ��ǣ�һ��ѡ������Ũ��ԼΪ_______%��
�ڵ�������NO��NO2��������Ӧ��ϵ����ʱ�ѵ�Ч����ѡ���������V(NO):V(NO2)=5 :3ʱ����ͨ��һ�����Ŀ�����ͬ��ͬѹ�£�V(����): V(NO)=___________ (���������������������ԼΪ20%)��

���𰸡� ���� ���� 2CO32-+SO2+H2O=2HCO3-+ SO32- 2Ba(NO3)2![]() 2BaO+O2��+4NO2�� BC C8H18(l)+ 12.5O2(g)= 8CO2(g)+9H2O(l) ��H=-5449.2kJ/mol 6 1:2
2BaO+O2��+4NO2�� BC C8H18(l)+ 12.5O2(g)= 8CO2(g)+9H2O(l) ��H=-5449.2kJ/mol 6 1:2
����������1����SO2�����е�S����sp2�ӻ������O�ɼ���SO2���ӹ�����V�Σ�����SO2�������ڼ��Է��ӣ����Ϸ�Ӧ������������̼���Ʒ�Ӧ�ģ����Բ���֤��S��C����Ԫ�صķǽ�����ǿ��������ͼ��֪��A���Ӧ��̼����Ũ����͡�̼������Ũ����ߣ����Է�Ӧ�����ӷ���ʽ��2CO32-+SO2+H2O=2HCO3-+ SO32-��
��2���������⼰��ͼ��Ϣ��֪��Ba(NO3)2�ֽ�Ϊ��������O2��NO2�� Ba(NO3)2�ֽⷴӦ�Ļ�ѧ����ʽΪ2Ba(NO3)2![]() 2BaO+O2��+4NO2�� ����A.ϡȼ���̵�Ŀ����Ϊ�˼�������β����NO��CO�ĺ�����A����ȷ��B.�����������У�Pt��BaO���ɿ���������B��ȷ��C.����β���������������еĵ�������ȿ����γɹ⻯ѧ������C��ȷ��D.��ȼ�����У�NO2��CO��Ӧ�Ļ�ѧ����ʽΪ2NO2 + 4CO == N2 + 4CO2����������ͻ�ԭ��������ʵ���֮��Ϊ4:1��D����ȷ������˵����ȷ����BC ����ʵ������ÿǧ��CxHy (��Һ��C8H18Ϊ��) ��O2�г��ȼ������Һ̬ˮ���ų�4.78��104kJ�������ɴ����1mol C8H18��ȫȼ�տ��Էų�5449.2kJ������������C8H18ȼ���ȵ��Ȼ�ѧ��Ӧ����ʽΪC8H18(l)+ 12.5O2(g)= 8CO2(g)+9H2O(l) ��H=-5449.2kJ/mol ��
2BaO+O2��+4NO2�� ����A.ϡȼ���̵�Ŀ����Ϊ�˼�������β����NO��CO�ĺ�����A����ȷ��B.�����������У�Pt��BaO���ɿ���������B��ȷ��C.����β���������������еĵ�������ȿ����γɹ⻯ѧ������C��ȷ��D.��ȼ�����У�NO2��CO��Ӧ�Ļ�ѧ����ʽΪ2NO2 + 4CO == N2 + 4CO2����������ͻ�ԭ��������ʵ���֮��Ϊ4:1��D����ȷ������˵����ȷ����BC ����ʵ������ÿǧ��CxHy (��Һ��C8H18Ϊ��) ��O2�г��ȼ������Һ̬ˮ���ų�4.78��104kJ�������ɴ����1mol C8H18��ȫȼ�տ��Էų�5449.2kJ������������C8H18ȼ���ȵ��Ȼ�ѧ��Ӧ����ʽΪC8H18(l)+ 12.5O2(g)= 8CO2(g)+9H2O(l) ��H=-5449.2kJ/mol ��
��3������ͼ��֪��������Ũ�ȴ���6%ʱ���ѵ�Ч�����ӵIJ������Է���������ԭ�ϵ�Ͷ�룬���ԴӾ��������Ͽ��ǣ�һ��ѡ������Ũ��ԼΪ6%.
�ڵ�������NO��NO2��������Ӧ��ϵ����1:1ʱ�ѵ�Ч����ѡ���������V(NO):V(NO2)=5 :3ʱ����NO��NO2������ֱ�Ϊ5L��3L������Ҫ��1L NOת��ΪNO2���������������1:1�Ĺ�ϵ����2NO+O2=2NO2��֪��ͬ��ͬѹ�£�1L NO��Ҫ0.5LO2�����������������������ԼΪ20%������Ҫ2.5L����������V(����): V(NO)=2.5:5= 1:2 ��