题目内容
【题目】某同学按图所示的装置进行电解实验。下列说法正确的是( )
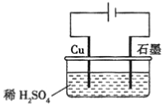
A. 电解过程中,铜极上有H2生成
B. 电解初期,主反应方程式为:2H2O=H2↑+O2↑
C. 整个电解过程中,H+的浓度不断增大
D. 电解一定时间后,石墨电极上有铜析出
【答案】D
【解析】由图可得,铜为阳极、石墨为阴极,电解开始阶段,阳极(铜电极)反应为Cu-2e-=Cu2+,阴极反应为2H++2e-=H2↑,电解总反应为:Cu+H2SO4![]() CuSO4+H2↑;A项,电解过程中,石墨极上有H2生成,故A错误;B项,由上述分析,电解初期主反应方程式为:Cu+H2SO4
CuSO4+H2↑;A项,电解过程中,石墨极上有H2生成,故A错误;B项,由上述分析,电解初期主反应方程式为:Cu+H2SO4![]() CuSO4+H2↑,故B错误;C项,电解过程中H+不断放电成为氢气,所以H+的浓度不断减小,故C错误;D项,随着反应的进行,溶液中Cu2+浓度增大,一段时间后,阴极上会发生反应Cu2++2e-=Cu,有铜析出,故D正确。
CuSO4+H2↑,故B错误;C项,电解过程中H+不断放电成为氢气,所以H+的浓度不断减小,故C错误;D项,随着反应的进行,溶液中Cu2+浓度增大,一段时间后,阴极上会发生反应Cu2++2e-=Cu,有铜析出,故D正确。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】在三个容积均为2L的密闭容器中发生反应:2HI(g)H2(g)+I2(g),已知H2(g)和I2(g)的起始物质的量均为0,HI(g)的物质的量随反应时间和温度的变化情况如表所示:
序号 | 时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
1 | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 |
2 | 800 | 1.0 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 |
3 | 820 | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 |
(1)实验1和实验2中使用了催化剂的实验是(填“1”或“2”);
(2)实验1中,0l0min内生成H2的平均反应速率为molL﹣1min﹣1;
(3)实验3的反应达到化学反应限度时,HI(g)转化率为 .