题目内容
【题目】用纯净的锌粒与稀盐酸反应制取氢气气体,请回答:
(1)实验过程如下图所示,分析判断段化学反应速率最快,段收集的氢气最多. 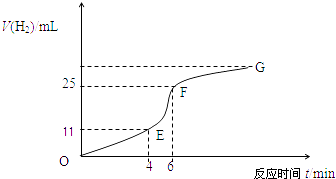
(2)将锌粒投入盛有稀盐酸的烧杯中,刚开始时产生H2的速率逐渐加快,其影响因素是 , 一定时间后反应速率逐渐减慢,其原因是 .
(3)为了减缓上述反应的速率,欲向溶液中加入下列物质,你认为可行的是
A.蒸馏水
B.氯化钠固体
C.氯化钠溶液
D.浓盐酸
E.降低温度
(4)EF段产生H2的反应速率为mLmin﹣1 .
【答案】
(1)EF;EF
(2)该反应是放热反应,温度升高,反应速率加快;随着反应的进行,盐酸的浓度逐渐减小,反应速率逐渐减小
(3)ACE
(4)7.0
【解析】解:(1.)根据纵坐标的高低判断收集气体的多少,纵坐标越高,收集的气体越大,所以是EF段;根据图象斜率判断反应速率的大小,斜率越大,反应速率越快,所以是EF段,所以答案是:EF段;EF段;
(2.)影响EF段速率变化主要因素是:该反应是放热反应,温度越高,反应速率越快,所以温度的改变是改变反应速率的主要原因;影响FG段速率变化主要因素是:随着反应的进行,盐酸的浓度逐渐减小,浓度越小,反应速率越小,所以浓度的改变是改变反应速率的主要原因;所以答案是:该反应是放热反应,温度升高,反应速率加快;随着反应的进行,盐酸的浓度逐渐减小,反应速率逐渐减小.
(3.)反应物的浓度越大,反应速率越快,所以只要使反应物浓度变小即可.
A、加蒸馏水,盐酸浓度变小,反应速率减小,故A正确;
B、加氯化钠固体,盐酸浓度不变,反应速率不变,故B错误;
C、加氯化钠溶液,溶液体积增大,盐酸浓度降低,反应速率减小,故C正确;
D、加浓盐酸,盐酸浓度增大,反应速率加快,故D错误;
E、温度降低,化学反应速率减小,故E正确;所以答案是:ACE;
(4.)因V= ![]() =
= ![]() =7.0mlmin﹣1 , 所以答案是:7.0.
=7.0mlmin﹣1 , 所以答案是:7.0.

 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案

