题目内容
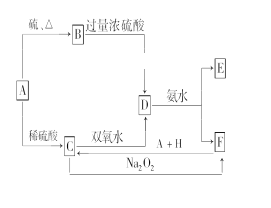
【题目】以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料生产铝和氮化铝的一种工艺流程如下【已知:SiO2在“碱溶”时转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀】。

(1)操作I、Ⅱ的名称为____________。
(2)用氧化物的形式表示铝硅酸钠的化学式_____________。
(3)溶液a中加入NaHCO3后,生成沉淀的离子方程式为____________。
(4)Al2O3比另外一种铝的化合物AlCl3熔点高出很多,原因是_________;有人考虑用熔融态AlCl3电解制备铝,你觉得是否可行,____(选填“可行”或“不可行”),试分析原因_________。
(5)取一定量的样品,用以下装置测定样品中AlN的纯度(夹持装置已略去)。打开K2,加入NaOH浓溶液,至不再产生NH3。打开K1,通入N2一段时间。

①实验中需要测定的数据是___________。
②由于装置存在缺陷,导致测定结果偏高,请提出改进方法:___________。
【答案】 过滤 Na2O·Al2O3·2SiO2·2nH2O AlO2-+HCO3-+H2O==Al(OH)3↓+CO32- Al2O3是离子晶体,AlCl3是分子晶体,离子键强于范德华力,所以Al2O3的熔点高 不可行 AlCl属于共价化合物,熔融状态不导电 AlN样品的质量以及装置C在吸收NH3前后的质量 在C后连接一个装有碱石灰的干燥管(或其他合理的干燥装置)
【解析】试题分析:由流程可知,铝土矿在碱溶时,SiO2转化为铝硅酸钠(NaAlSiO4·nH2O)沉淀分离出来,Al2O3转化为偏铝酸钠溶液,加入碳酸氢钠溶液时,偏铝酸钠转化为氢氧化铝沉淀,过滤后,把氢氧化铝分离出来加热灼烧,氢氧化铝分解为氧化铝,电解熔融的氧化铝得到铝。
(1)操作I、Ⅱ的名称为过滤。
(2)用氧化物的形式表示铝硅酸钠的化学式为Na2O·Al2O3·2SiO2·2nH2O。
(3)溶液a中加入NaHCO3后,生成沉淀的离子方程式为AlO2-+HCO3-+H2O==Al(OH)3↓+CO32- 。
(4)Al2O3比另外一种铝的化合物AlCl3熔点高出很多,原因是Al2O3是离子晶体,AlCl3是分子晶体,离子键强于范德华力,所以Al2O3的熔点高;用熔融态AlCl3电解制备铝是不可行的,因为AlCl3属于共价化合物,熔融状态不导电。
(5)由实验装置可知,AlN与NaOH浓溶液反应生成偏铝酸钠溶液和氨气,氨气经碱石灰干燥后被浓硫酸吸收,测出该装置的增重即可根据样品的质量求出样品中AlN的纯度。
①实验中需要测定的数据是AlN样品的质量以及装置C在吸收NH3前后的质量。
②C装置中的浓硫酸可以吸收空气中的水蒸气,导致测定结果偏高,改进方法为在C后连接一个装有碱石灰的干燥管(或其他合理的干燥装置)。

 阅读快车系列答案
阅读快车系列答案