题目内容
【题目】下列反应(均未配平)中,氧化剂与还原剂物质的量的关系为1∶2的是
A.Cu+H2SO4![]() CuSO4+SO2↑+H2O
CuSO4+SO2↑+H2O
B.CH3COOH+Ca(ClO)2![]() HClO+Ca(CH3COO)2
HClO+Ca(CH3COO)2
C.I2+NaClO3![]() NaIO3+Cl2
NaIO3+Cl2
D.HCl+MnO2![]() MnCl2+Cl2↑+H2O
MnCl2+Cl2↑+H2O
【答案】D
【解析】
据化合价变化判断氧化还原反应,分析氧化剂、还原剂。又据化合价升降总数相等,求氧化剂、还原剂的物质的量之比。
A. Cu元素化合价升高2,Cu是还原剂。S元素化合价降低2,H2SO4是氧化剂。氧化剂、还原剂的物质的量之比为1:1,A项错误;
B. CH3COOH与Ca(ClO)2发生复分解反应,不属于氧化还原反应,B项错误;
C. 碘元素化合价升高5,I2是还原剂。氯元素化合价降低,NaClO3是氧化剂。NaClO3与I2物质的量之比为2:1,C项错误;
D. 氯元素化合价升高1,HCl是还原剂。锰元素化合价降低2,MnO2是氧化剂。氧化剂、还原剂的物质的量之比为1:2,D项正确。
本题选D。

 阅读快车系列答案
阅读快车系列答案【题目】邻硝基甲苯和对硝基甲苯能被用作爆炸品检测的示踪剂。某探究小组利用下图反应和装置制备一硝基甲苯。
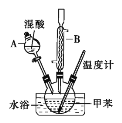
实验中可能用到的数据:
密度/g·cm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
实验步骤:
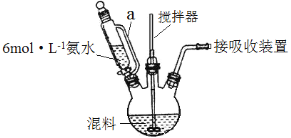
①按体积比1∶3配制浓硫酸与浓硝酸的混合物80mL;②在250mL的三颈烧瓶中加入30mL(26g)甲苯,按图所示装好药品和其他仪器;③向三颈烧瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);④控制温度约为50℃,反应大约10min,三颈烧瓶底有大量淡黄色油状液体出现;⑤分离出一硝基甲苯的总质量为27.20g。
请回答下列问题:
(1)使用仪器A前必须进行的操作是_______。
(2)该实验采用水浴加热,水浴加热的优点有:受热均匀、_______。
(3)配制混酸的方法是分别量取20mL浓硫酸和60mL浓硝酸,将浓_______倒入烧杯中,浓_______沿着烧杯内壁缓缓注入,并不断搅拌。
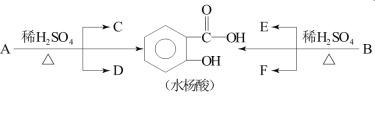
(4)控制温度约为50℃时,反应生成的产物一硝基甲苯是邻硝基甲苯和对硝基甲苯混合物,写出该反应生成对硝基甲苯的化学方程式_______。
(5)分离反应后产物的方案如下:

①操作1的名称为_______。
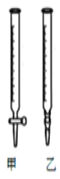
②操作2中,下列仪器选择及安装正确的是_______(填字母)。
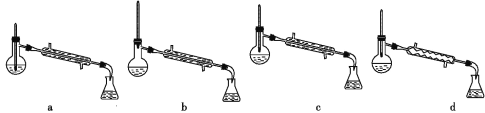
(6)该实验中一硝基甲苯的产率为_______(保留两位有效数字)。