ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩΘ®1Θ©Α±ΤχΜΙ‘≠ΒΣ―θΜ·ΈοΒΡΖ¥”ΠΈΣΘΚ
ΔΌN2(g)+O2(g)=2NO(g) ΓςH1
ΔΎ4NH3(g)+3O2(g)=2N2(g)+6H2O(l) ΓςH2
‘ρ4NH3(g)+6NO(g)=5N2(g)+6H2O(1) ΓςH=___ΓΘ(”ΟΚ§ΓςH1ΓΔΓςH2ΒΡ ΫΉ”±μ Ψ)
“άΨίΖ¥”ΠΔΎΘ§ΫΪΑ±Τχ…ηΦΤ≥…»ΦΝœΒγ≥ΊΘ§”ΟKOH»ή“ΚΉςΒγΫβ÷ »ή“ΚΘ§–¥≥ωΗΚΦΪΒγΦΪΖ¥”Π ΫΘΚ____ΓΘ
Θ®2Θ©“ΜΕ®Έ¬Ε»œ¬Θ§œρ2LΚψ»ίΟή±’»ίΤς÷–≥δ4.0molNO2ΚΆ4.0mol COΘ§‘Ύ¥ΏΜ·ΦΝΉς”Οœ¬ΖΔ…ζΖ¥”Π4CO(g)+2NO2(g)N2(g)+4CO2(g) ΓςHΘΦ0Θ§≤βΒΟœύΙΊ ΐΨί»γ±μΘΚ
0min | 5min | 10min | 15min | 20min | |
c(NO2)/molL1 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
c(N2)/molL1 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
ΔΌ05minΘ§”ΟNO2ΒΡ≈®Ε»±δΜ·±μ ΨΒΡΖ¥”ΠΥΌ¬ ΈΣ______ΓΘ
ΔΎ“‘œ¬±μ ωΡήΥΒΟςΗΟΖ¥”ΠΦΚ¥οΒΫΤΫΚβΉ¥Χ§ΒΡ «_____ΓΘ
AΘ°2v(NO2)’ΐ=v(N2)Ρφ BΘ°ΤχΧεΟήΕ»≤Μ‘Ό±δΜ·
CΘ°ΤχΧεΤΫΨυœύΕ‘Ζ÷Ή”÷ ΝΩ≤Μ‘Ό±δΜ· DΘ°N2”κCO2ΒΡΈο÷ ΒΡΝΩ÷°±»±Θ≥÷≤Μ±δ
Δέ20min ±Θ§±Θ≥÷Έ¬Ε»≤Μ±δΘ§ΦΧ–χœρΗΟ»ίΤς÷–Φ”»κ1.0molNO2ΚΆ1.0molCOΘ§Ζ¥”Π‘Ό¥Έ¥οΒΫΤΫΚβ ±Θ§NO2ΒΡΉΣΜ·¬ ±»‘≠ΤΫΚβ___(ΧνΓΑ‘ω¥σΓ±ΓΔΓΑΦθ–ΓΓ±ΜρΓΑ≤Μ±δ)ΓΘ
ΔήΗΟΈ¬Ε»œ¬Ζ¥”ΠΒΡΜ·―ßΤΫΚβ≥Θ ΐK=____ΓΘ
Θ®3Θ© ΣΖ®Ά―œθΘΚ≤…”ΟNaClO2»ή“ΚΉςΈΣΈϋ ’ΦΝΩ…Ε‘―ΧΤχΫχ––Ά―œθΓΘ323Kœ¬Θ§œρΉψΝΩΦν–‘NaClO2»ή“Κ÷–Ά®»κΚ§NOΒΡ―ΧΤχΘ§≥δΖ÷Ζ¥”ΠΚσΘ§»ή“Κ÷–άκΉ”≈®Ε»ΒΡΖ÷ΈωΫαΙϊ»γ±μΘΚ
άκΉ” | NO3 | NO2 | Cl |
c/(molL1) | 2.0ΓΝ104 | 1.0ΓΝ104 | 1.75ΓΝ104 |
ΔΌNaClO2»ή“Κœ‘Φν–‘Θ§”ΟάκΉ”ΖΫ≥Χ ΫΫβ Ά‘≠“ρ_____ΓΘ
ΔΎ“άΨί±μ÷– ΐΨίΘ§–¥≥ωNaClO2»ή“ΚΆ―œθΙΐ≥Χ÷–ΖΔ…ζΉήΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ Ϋ_____
ΓΨ¥πΑΗΓΩΓςH=ΓςH2Θ≠3ΓςH1 2NH3Θ≠6e+6OHΘΫN2+6H2O 0.06mol/(Lmin) C ‘ω¥σ 0.11 ClO2+H2OHClO2+OHΘΜ 12NO+7ClO2+12OHΘΫ8NO3+4NO2+7Cl+6H2O
ΓΨΫβΈωΓΩ
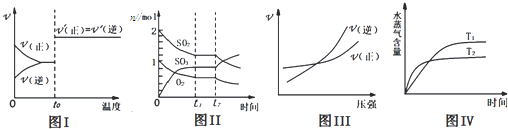
Θ®1Θ©“άΨίΗ«ΥΙΕ®¬…Ϋβ¥πΘΜ»ΦΝœΒγ≥Ί÷–Θ§Α±Τχ‘ΎΗΚΦΪ ßΒγΉ”ΉΣΜ·ΈΣΒΣΤχΘΜ
Θ®2Θ©ΔΌάϊ”ΟΥΌ¬ ΒΡΕ®“ε ΫΫβ¥πΘΜ
ΔΎ¥οΤΫΚβΉ¥Χ§ ±ΗςΉιΖ÷ΒΡΈο÷ ΒΡΝΩΓΔ≈®Ε»Β»≤ΜΥφ ±ΦδΒΡΗΡ±δΕχΗΡ±δΘΜ
Δέ20min ±Θ§œρ»ίΤς÷–Φ”»κ1.0molNO2ΚΆ1.0molCOΘ§œύΒ±”Ύ‘ω¥σ―Ι«ΩΘ§ΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ·ΘΜ
ΔήΜ·―ßΤΫΚβ≥Θ ΐKΒ»”ΎΤΫΚβ ±…ζ≥…Έο≈®Ε»Οί÷°Μΐ±»…œΖ¥”ΠΈο≈®Ε»Οί÷°ΜΐΘΜ
Θ®3Θ©ΔΌΗυΨί―ΈάύΥ°ΫβΒΡ‘≠άμΖ÷ΈωΘΜ
ΔΎœρΉψΝΩΦν–‘NaClO2»ή“Κ÷–Ά®»κΚ§NOΒΡ―ΧΤχΘ§≥δΖ÷Ζ¥”ΠΚσΘ§»ή“Κ÷–άκΉ”≈®Ε»ΒΡΖ÷ΈωΫαΙϊΒΟΒΫNO3-ΘΚNO2-ΘΚCl-=2ΘΚ1ΘΚ1.75=8ΘΚ4ΘΚ7Θ§ΫαΚœΒγΚ… ΊΚψΓΔΒγΉ” ΊΚψΚΆ‘≠Ή” ΊΚψ≈δΤΫ ι–¥άκΉ”ΖΫ≥Χ ΫΓΘ
Θ®1Θ©“άΨίΗ«ΥΙΕ®¬…Ω…÷ΣΘ§ΔΎ-3ΓΝΔΌΒΟ4NH3(g)+6NO(g)ΘΫ5N2(g)+6H2O(1)Θ§Ι ΓςH=ΓςH2Θ≠3ΓςH1ΘΜΗυΨίΖ¥”ΠΔΎΩ…÷ΣΘ§ΗΟ»ΦΝœΒγ≥Ί÷–KOH»ή“ΚΉςΒγΫβ÷ »ή“ΚΘ§Α±Τχ‘ΎΗΚΦΪ ßΒγΉ”ΖΔ…ζ―θΜ·Ζ¥”Π…ζ≥…ΒΣΤχΘ§ΤδΒγΦΪΖ¥”Π ΫΈΣΘΚ2NH3Θ≠6e+6OHΘΫN2+6H2OΘΜ
Θ®2Θ©ΔΌv(NO2)=![]() =
=![]() =0.06mol/(Lmin)ΘΜ
=0.06mol/(Lmin)ΘΜ
ΔΎAΘ°¥οΒΫΤΫΚβΉ¥Χ§ ±Θ§v(NO2)’ΐ=2v(N2)ΡφΘ§Aœν¥μΈσΘΜ
B. ”…”ΎΖ¥”ΠΈοΨυΈΣΤχΧεΘ§«“Ζ¥”Π«ΑΚσ÷ ΝΩ ΊΚψΘ§«“»ίΤςΈΣΚψ»ίΒΡ»ίΤςΘ§Ι ΤχΧεΟήΕ»“Μ÷±≤Μ±δΘ§Ι ΤχΧεΟήΕ»≤Μ±δ≤ΜΡήΥΒΟςΖ¥”Π «Ζώ¥οΤΫΚβΘ§Bœν¥μΈσΘΜ
C. ΤχΧεΤΫΨυœύΕ‘Ζ÷Ή”÷ ΝΩ‘Ύ ΐ÷Β…œΒ»”ΎΡΠΕϊ÷ ΝΩΘ§![]() Θ§”…”Ύ¥ΥΖ¥”ΠΒΡΖ¥”ΠΈοΚΆ…ζ≥…ΈοΨυΈΣΤχΧεΘ§Ι ΤχΧεΒΡΉή÷ ΝΩ“Μ÷±≤Μ±δΘ§Εχ¥ΥΖ¥”Π‘ΎΤΫΚβ÷°«ΑΤχΧεΒΡΈο÷ ΒΡΝΩ‘ΎΦθ–ΓΘ§Ι ΤΫΚβ÷°«ΑΤχΧεΒΡΤΫΨυœύΕ‘Ζ÷Ή”÷ ΝΩ‘Ύ‘ω¥σΘ§Β±≤Μ±δ ±‘ρΖ¥”Π¥οΤΫΚβΘ§Cœν’ΐ»ΖΘΜ
Θ§”…”Ύ¥ΥΖ¥”ΠΒΡΖ¥”ΠΈοΚΆ…ζ≥…ΈοΨυΈΣΤχΧεΘ§Ι ΤχΧεΒΡΉή÷ ΝΩ“Μ÷±≤Μ±δΘ§Εχ¥ΥΖ¥”Π‘ΎΤΫΚβ÷°«ΑΤχΧεΒΡΈο÷ ΒΡΝΩ‘ΎΦθ–ΓΘ§Ι ΤΫΚβ÷°«ΑΤχΧεΒΡΤΫΨυœύΕ‘Ζ÷Ή”÷ ΝΩ‘Ύ‘ω¥σΘ§Β±≤Μ±δ ±‘ρΖ¥”Π¥οΤΫΚβΘ§Cœν’ΐ»ΖΘΜ
D. ΗςΈο÷ ΒΡΈο÷ ΒΡΝΩ±Θ≥÷≤Μ±δΩ…ΥΒΟςΖ¥”Π¥οΒΫΤΫΚβΉ¥Χ§Θ§ΒΪN2”κCO2ΒΡΈο÷ ΒΡΝΩ÷°±»±Θ≥÷≤Μ±δ≤ΜΡήΥΒΟςΖ¥”Π¥οΒΫΤΫΚβΉ¥Χ§Θ§Dœν¥μΈσΘΜ
¥πΑΗΈΣΘΚCΘΜ
Δέ20min ±Θ§œρ»ίΤς÷–Φ”»κ1.0molNO2ΚΆ1.0molCOΘ§œύΒ±”Ύ‘ω¥σ―Ι«ΩΘ§ΤΫΚβœρ’ΐΖ¥”ΠΖΫœρ“ΤΕ·Θ§Υυ“‘NO2ΒΡΉΣΜ·¬ ±»‘≠ΤΫΚβ‘ω¥σΘ§Ι ¥πΑΗΈΣΘΚ‘ω¥σΘΜ
Δή 4COΘ®gΘ©+2NO2Θ®gΘ©N2Θ®gΘ©+4CO2Θ®gΘ©
≥θΤπ≈®Ε»ΘΚ2 2 0 0
±δΜ·≈®Ε»ΘΚ1 0.5 0.25 1
ΤΫΚβ≈®Ε»ΘΚ1 1.5 0.25 1
Υυ“‘K=![]() =0.11Θ§Ι ¥πΑΗΈΣΘΚ0.11ΘΜ
=0.11Θ§Ι ¥πΑΗΈΣΘΚ0.11ΘΜ
Θ®3Θ©ΔΌNaClO2»ή“Κœ‘Φν–‘ «“ρΈΣHClO2ΈΣ»θΥαΘ§ClO2-‘ΎΥ°»ή“Κ÷–ΜαΖΔ…ζΥ°ΫβΘ§ Ι»ή“Κœ‘Φν–‘Θ§ΤδΥ°ΫβΖΫ≥Χ ΫΈΣΘΚClO2+H2OHClO2+OHΘ§Ι ¥πΑΗΈΣΘΚClO2+H2OHClO2+OHΓΘ
ΔΎœρΉψΝΩΦν–‘NaClO2»ή“Κ÷–Ά®»κΚ§NOΒΡ―ΧΤχ,≥δΖ÷Ζ¥”ΠΚσ,»ή“Κ÷–άκΉ”≈®Ε»ΒΡΖ÷ΈωΫαΙϊΒΟΒΫNO3-ΘΚNO2-ΘΚCl-=2ΘΚ1ΘΚ1.75=8ΘΚ4ΘΚ7Θ§ΫαΚœΒγΚ… ΊΚψΓΔΒγΉ” ΊΚψΚΆ‘≠Ή” ΊΚψ≈δΤΫ ι–¥άκΉ”ΖΫ≥Χ ΫΈΣΘΚ12NO+7ClO2+12OHΘΫ8NO3+4NO2+7Cl