题目内容
4.等质量的镁和铝分别跟足量盐酸反应,生成的氢气的分子数之比为( )| A. | 1:1 | B. | 3:4 | C. | 3:2 | D. | 8:9 |
分析 根据n=$\frac{m}{M}$计算Mg、Al的物质的量之比,根据电子转移守恒可知,生成的氢气分子数目之比等于金属提供电子数目之比.
解答 解:根据n=$\frac{m}{M}$可知,等质量Mg、Al的物质的量之比=27g/mol:24g/mol=9:8,根据电子转移守恒可知,生成的氢气分子数目之比等于金属提供电子数目之比,故生成氢气分子数目之比=9×2:8×3=3:4,故选:B.
点评 本题考查化学方程式有关计算,题目利用守恒法进行解答,简化计算过程,可以利用赋值法根据方程式计算,难度不大.

练习册系列答案
相关题目
14.为验证物质的浓度对化学反应速率的影响,配制1mol•L-1的盐酸置于大烧杯中,并取3mL0.1mol•L-1的Na2S2O3溶液与3mL该盐酸反应,产生明显浑浊约需80s.第二天又用3mL 0.2mol•L-1的Na2S2O3溶液与原盐酸3mL反应,产生浑浊也需80s左右(已知:Na2S2O3+2HCl=2NaCl+S↓+SO2↑+H2O).下列关于该实验的评价及结论正确的是( )
| A. | 浓度对反应速率的影响不大 | |
| B. | 第二天所用的盐酸浓度较稀 | |
| C. | 该反应用盐酸表示的速率与用硫代硫酸钠表示的速率数值相等 | |
| D. | 任何化学反应,反应时间相同,化学反应速率均相同 |
12.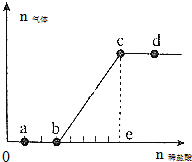 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.下列有关说法中正确的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.下列有关说法中正确的是( )
 向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.下列有关说法中正确的是( )
向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示.下列有关说法中正确的是( )| A. | a点对应的溶液中c(CO${\;}_{3}^{2-}$)>c(HCO${\;}_{3}^{-}$) | |
| B. | b,c段反应的离子方程式为HCO${\;}_{3}^{-}$+H+═H2O+CO2↑ | |
| C. | 原溶液中n(NaCO3)=n(NaHCO3) | |
| D. | K+、NO${\;}_{3}^{-}$、SiO${\;}_{3}^{2-}$可大量存在于d点对应的溶液中 |
19.有一在空气中暴露过久的NaOH固体,经分析得知其含水,Na2CO3•10H2O,Na2CO3,其余为NaOH,取此样品10.8g溶于100mL 1mol•L-1的硫酸里,剩余酸需加入0.4g NaOH刚好中和完全,由此可知蒸发中和后的溶液可得固体质量( )
| A. | 14.2g | B. | 19.8g | C. | 21.3g | D. | 无法计算 |
9.在0.1L某浓度的NaCl溶液中含有0.8mol Na+,下列对该溶液的说法中,不正确的是( )
| A. | 量取10mL该溶液倒入试管中,试管中,试管中Na+的物质的量为0.08mol | |
| B. | 该溶液的物质的量浓度为0.8mol•L-1 | |
| C. | 该溶液中含有46.8g NaCl | |
| D. | 配置50mL该溶液需用23.4g NaCl |
2.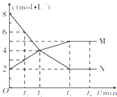 100℃时,密闭容器内某反应中各物质的物质的量浓度随反应时间变化的曲线如图所示,下列有关说法中正确的是( )
100℃时,密闭容器内某反应中各物质的物质的量浓度随反应时间变化的曲线如图所示,下列有关说法中正确的是( )
 100℃时,密闭容器内某反应中各物质的物质的量浓度随反应时间变化的曲线如图所示,下列有关说法中正确的是( )
100℃时,密闭容器内某反应中各物质的物质的量浓度随反应时间变化的曲线如图所示,下列有关说法中正确的是( )| A. | t2时刻,v(M)=v(N) | |
| B. | t3~t4时段内平均反应速率为0 | |
| C. | 该反应可表示为2N?M | |
| D. | 若反应在80℃时进行,则t1时c(N)<6mol•L-1 |
3.如图所示,试管中的物质M可能是( )
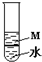

| A. | 四氯化碳 | B. | 乙醇 | C. | 已烷 | D. | 溴苯 |